|
İÇ HASTALIKLARI Dergisi 2011; 18: 181-223
DERLEME
|
Diabetes Mellitus Tanı ve Tedavisinde Güncel Durum
Up to Date on Diagnosis and Treatment of Diabetes Mellitus
Prof. Dr. Nevin DİNÇÇAĞ
İstanbul Üniversitesi İstanbul Tıp Fakültesi, İç Hastalıkları
Anabilim Dalı, Endokrinoloji ve
Metabolizma Hastalıkları Bilim Dalı, İstanbul
ÖZET
Diabetes mellitus insülin eksikliği ya da etkisindeki defektler nedeniyle organizmanın karbonhidrat, yağ ve proteinlerden yeterince yararlanamadığı, sürekli tıbbi bakım gerektiren, kronik metabolizma hastalığıdır. Tüm dünyadaki gibi ülkemizde de giderek artan prevalansın yol açtığı yüksek maliyet ve akut ya da kronik dönemde oluşturduğu komplikasyonları nedeniyle iyi tedavi edilmelidir. Tedavide amaç, gün içerisinde glisemik kontrolün sağlanması , akut komplikasyon gelişme riskinin azaltılması, mikro ve makrovasküler komplikasyonların önlenmesi, eşlik eden diğer sorunların düzeltilmesi ve böylelikle diyabetlide yaşam kalitesinin düzeltilmesidir. Bu makalede diyabetin tanımı, tanı kriterleri ve tedavi ilkeleri güncel bilgiler ışığında özetlenmiştir.
Anahtar Kelimeler: Hiperglisemi, tip 1 diyabet, tip 2 diyabet, oral antidiyabetik ilaçlar, insülin
SUMMARY
Diabetes mellitus is a chronic illness that requires continuing medical care and ongoing patient self-management education and support to prevent acute complications and to reduce the risk of long-term complications. Prevalence of diabetes is growing in our country similar like in all over the world. Diabetes mellitus affects more than 6.5 million people in Turkey and is a chronic condition heavily influenced by patient self-management and follow-up with a variety of health care providers. Providers need to have a basic understanding of potential benefits of specific solutions for their patients and best clinical practice and integrate with their practice flow. You can find some update information’s about diagnosis and treatment of diabetes mellitus in this article.
Key Words: Hyperglycemia, type 1 diabetes, type 2 diabetes, oral anti-diabetic therapy, insulin therapy
Diabetes mellitus (diyabet), insülin eksikliği ya da etkisindeki defektler nedeniyle organizmanın karbonhidrat, yağ ve proteinlerden yeterince yararlanamadığı, sürekli tıbbi bakım gerektiren, kronik metabolizma hastalığıdır. Görülme sıklığının artışı önemlidir; artan prevalansın yol açtığı yüksek maliyet ve akut ya da kronik dönemde oluşturduğu komplikasyonları nedeniyle iyi tedavi edilmelidir. Tedavide amaç; gün içerisinde glisemik kontrolün sağlanması, akut komplikasyon gelişim riskinin azaltılması, mikrovasküler ve makrovasküler kronik komplikasyonların önlenmesi, eşlik eden diğer sorunların düzeltilmesi ve böylelikle diyabetlide yaşam kalitesinin yükseltilmesidir. İyi tedavi edebilmenin ön şartı hastalığı doğru tanıma ve sınıflandırmadır. Bu makalede diyabetin tanımı, tanı kriterleri ve tedavi ilkeleri güncel bilgiler ışığında özetlenecektir.
I. DİYABETİN TANIMLAMASI ve TANINMASI
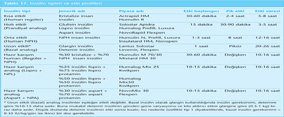
Son 10 yılda diyabet tanı ve sınıflamasında glukoz metabolizmasındaki diğer bozuklukları da kapsayacak şekilde değişiklikler yapılmıştır. Önce 1997 yılında Amerikan Diyabet Birliği (ADA) yeni tanı ve sınıflama kriterleri yayınlamış, ardından 1999 yılında Dünya Sağlık Örgütü (DSÖ) yayınlanan tanı kriterlerini küçük revizyonlarla kabul etmiştir. 2003 yılında ADA, bozulmuş açlık glisemisi (IFG) tanımını ekleyerek diyabet tanımında revizyona gitmiştir. DSÖ ve Uluslararası Diyabet Federasyonu (IDF) ise 2006 yılındaki raporlarında 1999 kriterlerinin korunmasını benimserken; ADA ve Avrupa Diyabet Çalışma Birliği (EASD) 2007 yılındaki son konsensus raporunda 2003 yılındaki düzenlemenin değişmemesi gerektiğini savunmaktadır. Günümüzde diyabet tanımlaması için geçerli olan bu düzenlemedir (Tablo 1).
Tablo 1’den anlaşılacağı üzere diyabet tanısında dört yöntem geçerlidir. Çok ağır semptomların olduğu durumlar dışında tanının ertesi gün bir başka yöntemle doğrulanması gerekir. Tanıda duyarlılığı ve özgüllüğü daha yüksek olan 75 g glukoz ile oral glukoz tolerans testi (OGTT) yapılmasıdır; ancak bu yöntemin aynı kişide bile günden güne değişkenliğinin yüksek olması, yoğun emek ve maliyet gerektirmesi kullanımını güçleştirmektedir. Buna karşın açlık glisemisinin daha kolay uygulanabilmesi ve ucuz olması pratikte kullanımını artırmaktadır. Tanı kriterlerinde esas alınan, venöz plazmada glukoz oksidaz yöntemiyle yapılan ölçüm değerleridir. Klinikte ya da hastaların ev ölçümlerinde kullandıkları tam kan, kapiller kan ve serum örneklerinde glisemi değerleri Tablo 2’de belirtilen formüllerde gösterildiği gibi biraz daha düşüktür. Ancak, son yıllarda kapiller kan ölçümü yapan cihazların plazma glukoz düzeylerine göre kalibre edilerek kullanılması benimsenmektedir.
HbA1C (A1C)’nin standardizasyonundaki sorunlar ve tanı eşiğindeki belirsizlik nedeniyle uzun yıllardır tanı amaçlı kullanılması önerilmemekteydi. Ancak ADA, EASD, IDF ve Uluslararası Kimyacılar Federasyonu (IFCC) temsilcilerinin oluşturduğu bir komitenin 2008 yılından beri yaptıkları bir dizi çalışma sonrasında, uluslararası standardizasyon kurallarını sağlamak koşuluyla diyabet tanısı için kesim noktasını %6.5 (48 mmol/mol) olarak belirlemişler ve A1C değerinin > %6.5, açlık plazma glukozu değerinin > 126 mg/dL olduğu durumların diyabet olarak kabul edilmesini ve A1C değerinin standart OGT’ye alternatif bir tanı yöntemi olarak benimsenmesini önermişlerdir. Bu öneri, A1C ölçümünün henüz her merkezde standardizasyona uygunluğunun sağlanamadığı düşünülürse, ülkemiz koşullarında şimdilik geçerli değildir.
Tablo 1’de belirtilen IFG ve bozulmuş glukoz toleransı (IGT), önceki yıllarda “latent diyabet”, “şimik diyabet”, “sınırda diyabet” olarak adlandırılmıştı. Bugün “prediyabet” olarak kabul edilen bu tanımlamalar, diyabet ve kardiyovasküler hastalık gelişiminde önemli risk faktörleridir. Günümüzde “izole IFG”, “izole IGT” ve “kombine IFG + IGT” kavramları kabul görmektedir. Tanımlamalar Tablo 1’den de anlaşıldığı gibi “izole IFG” açlık plazma glukozunun 100-125 mg/dL ve ikinci saat plazma glukozunun < 140 mg/dL; “izole IGT” ise açlık plazma glukozu < 100 mg/dL ve ikinci saat plazma glukozunun 140-199 mg/dL olması durumudur. Kombine IFG + IGT durumu glukoz metabolizmasının daha ileri düzeyde bozukluğunu ifade eder. Bu durumda hem açlık plazma glukozu 100-125 mg/dL, hem de ikinci saat plazma glukozu 140-199 mg/dL düzeyindedir.
Özetle ülkemizde diyabet tanısında, Türkiye Endokrinoloji ve Metabolizma Hastalıkları Derneği (TEMD) tarafından önerilen yaklaşım şudur:
• Yaşam tarzı diyabet sıklığını artıracak yönde hızla değişen toplumumuzda, diyabet bilincinin yerleştirilmesi açısından Tablo 1’de özetlenen 2003 yılı prediyabet kriterlerinin korunması gerektiği uygun bulunmaktadır.
• A1C’nin teknik ve standardizasyonundaki eksiklikler dikkate alındığında, ülkemizde testin bu amaçla kullanılması, şu an için uygun görülmemektedir.
II. DİYABET SEMPTOMLARI
Diyabet genellikle Tablo 3’te belirtilen semptomlarla aşikar hale geçer. Tanıda özellikle daha az görülen semptomların varlığı dikkate alınmalıdır.
III. DİYABETİN SINIFLANDIRILMASI
Diyabet tanısı alan hastada diyabet sınıflaması, klinik ve laboratuvar bulgularına göre yapılır. Tablo 4’te özetlenen diyabet sınıflamasında dört klinik tip yer almaktadır. Bunların üçü [Tip 1 diyabet, Tip 2 diyabet ve gestasyonel diyabet] primer, diğerleri (spesifik diyabet tipler) sekonder diyabet formları olarak bilinmektedir.
İyi bir glisemik kontrol sağlayabilmek için herşeyden önce diyabet tiplemesinin doğru yapıldığından emin olmak gerekir. Yeni tanı almış 5102 Tip 2 diyabet hastasının 20 yıl izlendiği Birleşik Krallık İleriye Dönük Diyabet Çalışması (United Kingdom Prospective Diabetes Study: UKPDS)’nda hastaların %11’inde pankreas adacık antikorlarının bulunduğu ve bu olguların çoğunda ilk birkaç yıl içinde insülin gereksiniminin ortaya çıktığı bildirilmiştir. Bu nedenle ileri yaşta ortaya çıkan, zayıf diyabetlilerde “Latent Autoimmun Diabetes of Adults (LADA)” ya da yavaş seyirli tip 1 diyabet (veya tip 1.5) adı verilen bu tanımlama akla getirilmelidir. Ayrıca, günümüzde obezitenin genç ve adölesan yaşlara kayması fenotipik olarak Tip 2 diyabete uyan olgularla da karşılaşmamıza yol açmaktadır. Literatürde tip 3 diyabet, dual diyabet, hibrid diyabet, duble diyabet gibi adlarla tanımlanan bu olguların da tanınması ve tedavileri özel bir dikkat ve beceri gerektirmektedir. Tip 1 ve Tip 2 diyabet ile aynı belirti ve bulguları saptanabilen Tip 3 diyabet tanısında dikkate alınması gereken özellikler şunlardır: Hastada obeziteyle ilişkili olarak insülin direnci belirtilerinin yanı sıra otoimmüniteyle ilişkili olarak pankreas adacık hücrelerine karşı otoantikorlar da mevcuttur ve tedavide insülin ve insülin direncine yönelik ajanların beraber kullanımı gerekebilir.
1. TİP 1 DİYABET
Fizyopatolojisi
Mutlak insülin eksikliği vardır. Hastaların %90’ında otoimmün (tip 1A), %10 kadarında nonimmün (tip 1B) beta-hücre yıkımı vardır.
Tip 1A diyabet: Riskli doku grubu yatkınlığı zemininde çevresel tetikleyici faktörler (virüs, toksin, emosyonel stres vs.) ile tetiklenen otoimmünitenin pankreas beta-hücrelerini harap etmesidir. Beta-hücre hasarı ilerleyicidir. Beta-hücre kitlesi %80-90 oranında azaldığında klinik diyabet semptomları ortaya çıkar. Başlangıçta otoantikorlar pozitif bulunur.
Tip 1B diyabet: Otoimmünite dışındaki bazı nedenlerden dolayı mutlak insülin eksikliği sonucu gelişir. Otoantikorlar saptanmaz.
Özellikleri
• İlerleyici beta-hücre harabiyetinin yıkım hızı ortaya çıkış yaşını belirler. Genellikle 30 yaşından önce başlar. Okul öncesi, puberte ve geç adölesan olmak üzere üç yaş grubunda pik yapar. Ancak yıkımın daha yavaş olduğu durumda klinik belirtilerin ortaya çıkışı daha ileri yaşlarda görülür. İleri yaşta görülen bu formu LADA ya da tip 1.5 olarak tanımlanır; azımsanmayacak sıklıkta olup, çocukluk çağı diyabete yakın oranda görüldüğü bildirilmektedir.
• Genelde ailede diyabetli yoktur.
• Hiperglisemiye ilişkin semptomlar ve bulgular aniden ortaya çıkar.
• Hastalar genellikle zayıf ya da normal kilodadır.
• Hasta diyabetik ketoasidoza yatkındırlar.
Tedavisi
Mutlak eksik olanı, yani insülini yerine koyma tedavisidir. 1911 yılında insülinin keşfi, Tip 1 diyabetli bireye yaşama hakkı sağlamıştır. İnsülin enjeksiyonlarının (enjektör, kalem ya da pompa) yanı sıra eğitim, tıbbi beslenme tedavisi ve egzersiz önemli tedavi basamaklarıdır. İnsülin tedavisi ileri bölümlerde detaylı olarak aktarılacaktır.
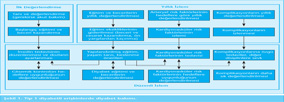
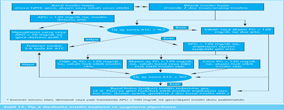
Tip 1 diyabetliler için tanımlanan ve önerilen diyabet bakım algoritması “ilk değerlendirme, yıllık izlem ve düzenli izlem” başlıkları altında Şekil 1’de gösterilmiştir.
2. TİP 2 DİYABET
Yaşam tarzının değişmesi ve yaşam süresinin uzaması nedeniyle sıklığı giderek artan bir hastalıktır. IDF tarafından yayınlanan son Diyabet Atlasına göre 2011 yılı sonu itibarıyla dünyada 20-79 yaş grubundaki diyabet nüfusunun 366 milyona ulaştığı ve bu sayının 2030 yılına kadar %51 artış ile 552 milyona varacağı tahmin edilmektedir. Ülkemizde de diyabet prevalansındaki artış hızı, dünya ülkelerinden geri kalmamaktadır. Türkiye’de 20 yaş ve üzerinde olan bireyleri kapsayan, 1998 yılında yapılmış TURDEP-I çalışmasında %7.2 olan diyabet prevalansı, 2010 yılında aynı merkezlerde tekrarlanan TURDEP-II çalışmasına göre %90 artış ile %13.7 düzeyine ulaşmıştır. Bu rakam, diyabet nüfusumuzun 6.5 milyonu aştığına işaret etmektedir.
Fizyopatolojisi
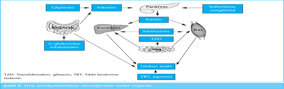
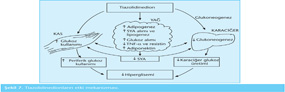
İlerleyici bir hastalık olan Tip 2 diyabette poligenetik olarak formatlanmış başlıca iki temel defekt söz konusudur. Bunlar; insülin direnci ve beta-hücresinde insülin sekresyon defektidir. Son yıllarda inkretin hormonların eksikliğinin yol açtığı glukagon yüksekliğinin de Tip 2 diyabet fizyopatolojisinde rol aldığı gösterilmiştir.
İnsülin direnci, hücre-reseptör defektidir; buna bağlı olarak organizmanın ürettiği insülinin kullanımında sorun vardır; bu nedenle glukoz hücre içine alınıp enerji olarak kullanılamaz. Beta-hücresindeki insülin sekresyon defekti nedeniyle de kan glukoz düzeyine yanıt olarak beklenen yeterli insülin salgılanamaz. Bu iki defekt birbirini kompanse ettiği sürece hastalık aşikar hale geçmez. Ancak beslenme düzeni, fiziksel inaktivite, stres ya da ilaç gibi çevresel faktörler nedeniyle defektler arasındaki kompansasyon bozulduğunda diyabet belirtileri ortaya çıkmaya başlar.
Hastalığın ortaya çıkmasından yıllarca öncesinde, kas ve karaciğer gibi ana hedef organlarda mevcut olan insülin direnci nedeniyle yeterince kullanılamayan glukoz, esasen defektli olan pankreas beta-hücrelerini aşırı çalışmaya zorlar; böylelikle artan hiperinsülinemi nedeniyle normoglisemi sürdürülür. Tam bu dönemde periferik kanda insülin düzeyi ölçülürse, aslında normal kabul edilen düzeyden daha yüksek değerlerde (hiperinsülinemi) olduğu saptanabilir. Fakat hastalığın doğal sürecinde yük altında çalışmakta olan pankreas beta-hücrelerinden insülin sekresyonu giderek azalmaya başlar ve öncelikle toklukta olmak üzere glisemi düzeyleri artmaya başlar; klinik belirtiler (yemek sonrası uyku hali, halsizlik ya da reaktif hipoglisemi semptomları) ortaya çıkar.
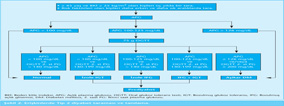
Kural olarak insülin direnci olan hastalarda diyabetin aşikar hale gelmeden önceki döneminde insülin direnci sendromu (IRS) veya metabolik sendrom mevcuttur. İnsülin direnci sendromu veya metabolik sendrom olarak tanımlanan klinik tabloda bazı klinik ve biyokimyasal özellikler, örneğin; santral (viseral) obezite, hipertansiyon, dislipidemi (yüksek trigliserid, düşük HDL-kolesterol, yüksek LDL-kolesterol), disglisemi ve hiperürisemi gibi durumların biri ya da birkaçı birlikte saptanabilir. Metabolik sendrom üzerinden gelişen farklı mekanizmalar endotel disfonksiyonuna yol açarak hiperkoagülabilite ve vasküler inflamasyona sebep olur; bu da diyabeti preklinik dönemden başlayarak kardiyovasküler hastalık eşdeğeri haline getirir. Hastalığın doğal seyri, sağlıklı yaşam biçimine dönüşüm tedbirleriyle durdurulamazsa, süreç içinde beta-hücrelerinin yıkımı artacak, yüksek kan şekeri değerleri yalnızca postprandiyal dönemde değil, açlık ve yemek öncesinde de saptanır hale gelecektir. Tablo kontrolsüz hiperglisemi haline dönüştüğünde, ateroskleroz hızlanacak, bulguları da kardiyovasküler hastalık kliniği olarak karşımıza çıkacaktır. Bu dönem öncesinde riskli hastaları tarama ve tanılama önemlidir. Erişkinlerde Tip 2 diyabet tarama ve tanılaması Şekil 2’de gösterilmiştir.
Prediyabet döneminde tanınması gereken bireylerin, yani Tip 2 diyabet açısından değerlendirilmesi gereken riskli adayların özellikleri şöyle sıralanabilir:
• Obez veya kilolu [beden kitle indeksi (BKİ) ≥ 25 kg/m2] ve özellikle santral obezitesi (bel çevresi kadında > 88 cm, erkekte > 102 cm) olan kişilerde, 45 yaşından itibaren, üç yılda bir, tercihan APG ile diyabet taraması yapılmalıdır.
• Ayrıca, BKİ ≥ 25 kg/m2 olan kişilerin aşağıdaki risk gruplarından birine mensup olmaları halinde, daha genç yaşlardan itibaren ve daha sık araştırılmaları gerekir.
- Birinci derece yakınlarında diyabet bulunanlar,
- Diyabet prevalansı yüksek etnik gruplara mensup kişiler,
- İri bebek doğuran veya obstetrik öyküsünde gestasyonel diyabet olanlar,
- Polikistik over sendromu olan kadınlar,
- Hipertansif bireyler (kan basıncı ≥ 140/90 mmHg),
- Dislipidemisi bulunanlar (HDL-kolesterol ≤ 35 mg/dL veya trigliserid ≥ 250 mg/dL),
- Daha önce IFG veya IGT saptanan bireyler,
- İnsülin direnci sendromu ile ilişkili klinik hastalığı ya da bulgusu (acanthosis nigricans) olanlar,
- Koroner, periferik veya serebrovasküler arter hastalığı bulunanlar,
- Düşük doğum tartısıyla doğmuş olanlar,
- Sedanter yaşamı ya da fizik aktivitesi az olan bireyler,
- Doymuş yağlardan zengin ve posa miktarı düşük beslenme alışkanlığı olanlar,
- Şizofreni veya başka bir sebeple antipsikotik ilaç kullanan kişiler.
Aşikar Tip 2 diyabetli hastaların tanı başlangıcında, %80’inde insülin direnci vardır; beta-hücre fonksiyonu %50 kaybolmuştur.
Klinik Özellikleri
• Çoğunlukla 30 yaşından sonra başlar; ancak son yıllarda obezite artışının sonucu olarak çocukluk ya da adölesan döneminde ortaya çıkan Tip 2 diyabet olgu sayısında artış vardır.
• Güçlü genetik yatkınlık söz konusudur ve ailede diyabetli sayısı arttıkça hastalığın ortaya çıkış yaşı küçülmektedir.
• Hastalar sıklıkla obez ya da kiloludur (BKİ > 25 kg/m2).
• Genellikle sinsi başlangıçlı olup, pek çok hastada uzun yıllar hiçbir semptom yoktur. Bazı hastalar bulanık görme, kaşıntı, el ve ayaklarda uyuşma ve karıncalanma, ayak ağrıları, tekrarlayan mantar infeksiyonları veya yara iyileşmesinde gecikme nedeniyle başvurabilir.
• Başlangıçta diyabetik ketoasidoza yatkınlık yoktur. Uzun süreli hiperglisemik seyirde ya da beta- hücre rezervinin azaldığı dönemlerde diyabetik ketoasidoz görülebilir.
Tedavisi
Yeni tanı konulmuş Tip 2 diyabetlilerin 20 yıl izlendiği UKPDS çalışması sonuçları göstermiştir ki, metabolik kontrol göstergesi olan A1C düzeyinde %1’lik iyileşme sağlanmasıyla diyabetik mikrovasküler komplikasyonların riski %35 oranında azalmaktadır. Çalışma sonunda makrovasküler komplikasyonların önlenmesi yönünde, hiperglisemi kontrolünün anlamlı bir etkisinin olmadığı bildirilmiştir; ancak aynı çalışmanın bitiminden 10 yıl sonraki takip verilerinde; başlangıçta yoğun biçimde tedavi edilen grupta makrovasküler komplikasyon gelişme riskinin ve mortalitenin daha az olduğu gözlenmiş; bu da çalışmayı yürüten araştırıcılar tarafından iyi glisemik kontrol sağlanmasının metabolik miras etkisi (metabolik hafıza) olarak yorumlanmıştır. O halde, Tip 2 diyabet tedavisinde temel amaç, en erken dönemde metabolik kontrolün sağlanmasıdır. Gün içerisinde glisemik kontrolün sağlanması ile akut komplikasyon gelişim riskinin azaltılması, mikrovasküler ve makrovasküler kronik komplikasyonların önlenmesi, eşlik eden obezite, hipertansiyon gibi diğer sorunların düzeltilmesi ve böylelikle diyabetlide yaşam kalitesinin yükseltilmesidir.
Bu nedenle günümüzde, tüm dünyada daha erken ve daha agresif tedavi önerilmektedir. Tedavide ilk basamaktan itibaren her aşamada, egzersiz ve vücut ağırlığının normale gelmesini sağlayan tıbbi beslenme tedavisi ön planda ele alınmalıdır. Tıbbi beslenme tedavisiyle, hastanın tüm hayatı boyunca uygulayabileceği en ideal ve kişiye özel beslenme düzeninin sağlanması hedeflenmelidir. Yakın geçmişe kadar Tip 2 diyabet tedavisinde ilk basamak olarak tıbbi beslenme tedavisi uygulamaları önerilmekteydi. Ancak, uzun vadede bu önlemler metabolik kontrolü sağlamada yetersiz kaldığı için hastaların çoğu kısa sürede en azından bir oral antidiyabetik ilaç tedavisine ihtiyaç duymaktaydı.
Günümüz pratiğinde de hala birçok meslektaşımız tarafından benimsenen eğilime göre, tıbbi beslenme tedavisi ve fiziksel aktiviteyi artırmaya yönelik yaşam tarzı değişikliği ile diyabeti kontrol altına alınamayan hastalara hala basamaklı tedavi uygulanmaktadır. İlk basamakta tedaviye bir oral antidiyabetik ilaçla başlanır; daha sonraki aşamalarda kural olarak farklı mekanizmaları olan, farklı sınıftan ajanlarla kombinasyon tedavisine geçilir, hastalık ilerlediğinde oral antidiyabetik ilaçlara insülin tedavisi eklenebilir veya tedaviye yalnızca insülinle devam edilir. Ancak basamaklı tedavinin komplikasyon gelişimini önlemedeki yetersizliği gösterildiğinden beri, tedavideki güncel öneri; sağlıklı yaşam tarzı değişimi önerilerine ek olarak fizyopatolojik temele yönelik, farklı etki mekanizmaları olan ilaçların kombinasyonuyla mümkün olduğunca erken bir tedavi başlanmasıdır. Tip 2 diyabette kullanılan oral antidiyabetik ilaçların detayları oral antidiyabetik ilaçlar bölümünde anlatılacaktır.
3. GESTASYONEL DİYABET
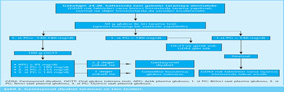
Gebelikte başlayan, genellikle doğumla birlikte sonlanan diyabet olarak tanımlanır. Aslında, genetik yatkınlık zemininde esasen var olan ve plasental hormonlar nedeniyle dekompanse hale geçen insülin direncidir. Sıklığı ve önemi gereği sınıflandırmada ayrı bir grup olarak tanımlanmaktadır. Genellikle asemptomatiktir. Ancak anne adayında yaşın ≥ 25 olması, gebelik öncesinde obezite, birinci derece akrabalarında diyabet öyküsü veya kötü obstetrik hikaye varlığı gestasyonel diyabet gelişmesinde risk faktörleridir. Bu nedenle gestasyonel diyabet Şekil 3’te gösterildiği biçimde her gebede, özellikle riskli olanlarda tarama testiyle araştırılmalıdır. Tedavisi, tıbbi beslenme tedavisi ve egzersiz programıdır. İzlemde hedef glisemi açlık plazma glukozu < 95 mg/dL, birinci saat plazma glukozu < 130 mg/dL olmalıdır. Hedef glisemisi tıbbi beslenme tedavisiyle kontrol altına alınamayan olgularda insülin uygulanır. Doğumla birlikte 1/3 olguda gestasyonel diyabet düzelir, kalan 2/3’de aşikar diyabet ya da glukoz intoleransı (IFG ya da IGT) devam edebilir. Bu nedenle postpartum dönemde 6-12. haftada 75 g glukozlu OGTT ile karbonhidrat metabolizması tetkik edilmelidir. Çünkü gestasyonel diyabet öyküsü ileri dönemlerde Tip 2 diyabet için önemli bir risk faktörüdür.
4. SPESİFİK DİYABET TİPLERİ
Diyabet tanısı alan bir bireyde, yaklaşımda ikinci basamak, hangi tip diyabet olduğunun kararıdır. Kriterlerin Tip 1 diyabet ya da Tip 2 diyabet yönünde net olmadığı durumlarda akla getirilmesi gereken Tablo 4’te belirtilen spesifik diyabet tipleridir. Sıklığı hiç de az olmayan formlar arasında MODY (Maturity Onset Diabetes of Youngs) başı çekmektedir.
- MODY monogenik diyabet formlarındandır. Bilinen 10 tipi mevcuttur; her birinde farklı bir kromozomun bir bölgesinde otozomal, dominant iletilen bir defekt mevcuttur. MODY olan bir diyabetlide en önemli özellikler şöyle özetlenebilir.
• Hastalar genellikle 30 yaşın altındadır (bazı hastalarda başlangıç yaşı < 50).
• Birinci derece akrabalarda benzer diyabet tablosu vardır.
• Hastalarda ağır obezite yoktur (bazen kilolu veya hafif obez olabilir); ayrıca metabolik sendrom, hipertansiyon, hiperlipidemi, polikistik over sendromu gibi insülin direnci belirtileri yoktur veya nadirdir.
• Bazı tiplerinde altı aylıktan önce başlayan kalıcı neonatal diyabet veya Tip 1 diyabet tablosu olabilirse de genelde Tip 2 diyabet kliniği gibi hafif-orta düzeyde hiperglisemi (130-250 mg/dL) ile seyreder.
• Genelde insülin ihtiyacı azdır (< 0.3 U/kg/gün); tedavide genellikle oral antidiyabetik ilaç yeterlidir.
• Hasta ve ailesinde adacık otoantikorları ve diğer otoimmün hastalıkların otoantikorları, (örn. tiroidit, pernisiyoza vs.) bulunmaz.
• Hasta ve yakınlarında kistik böbrek hastalığı bulunabilir.
- Monogenik diyabet formlarına bir başka örnek, mitokondriyal diyabettir. Mitokondriyal diyabet, mitokondriyal genomdaki mutasyonlarla ilişkili insülin sekresyon bozukluğuyla seyreden monogenik diyabet formudur. Özellikleri şöyle özetlenebilir:
• Maternal kalıtım gösterir, çoğunlukla kadınlarda görülür.
• Klinik olarak asemptomatik olgulardan yavaş seyirli ya da hızla insülin gereksinimine ilerleyen beta-hücre defektine kadar değişebilen farklı tablolar gösterebilir.
• Sensöriyal hipoakuzi gibi ekstrapankreatik belirtiler karakteristiktir. Bu nedenle MIDD (Maternally Inherited Diabetes with Deafness) olarak adlandırılır.
• MIDD’da en sık görülen mutasyon, mitokondriyal genomun m.3243 A > G pozisyonundaki nokta mutasyondur; MIDD, farklı bir sendrom olan MELAS (mitokondriyal miyopati, ensefalopati, laktik asidoz ve stroke benzeri ataklar) ile de ilişkilendirilmektedir.
- Spesifik diyabet tiplerine sıkça rastladığımız bir başka örnek, ilaçların yol açtığı diyabet formudur. Özellikle stresin günlük yaşantımızın bir parçası haline gelmesiyle birlikte, giderek daha çok insan genç yaşlardan itibaren depresyon ve psikoz gibi sorunlarla karşılaşmakta ve antipsikotik ilaçların kullanımı artmaktadır. Bu ilaçları, insülin direnci başta olmak üzere, metabolik yan etkilerinin hekimler tarafından iyi bilinmemesi ya da hasta yoğunluğu nedeniyle hastaların uyarılmaması nedeniyle acil polikliniklere ilk kez diyabetik ketoasidoz ile ortaya çıkan, Tip 2 diyabet kliniğinde genç hastaların başvurusunu artırmıştır.
Diyabet tipinin belirlenmesinde dikkate alınması gereken parametreler Tablo 5’te gösterilmiştir.
Özet olarak diyabetin sınıflandırılmasında;
Tanısı diabetes mellitus olarak doğrulanmış bir kişide bir sonraki basamak, hangi tip diyabet olduğunun belirlenmesidir. Diyabet tipleri ayırıcı tanısında belirleyici olan aşağıdaki kriterler dikkate alınmalıdır.
- Yaş,
- Ailede diyabet öyküsünün sorgulanması,
- Bireyin BKİ’si,
- İnsülin direnci sendromu komponentlerinden (obezite, hipertansiyon, dislipidemi, polikistik over sendromu, kardiyovasküler hastalık vs.) biri ya da birkaçının araştırılması,
- Endojen insülin (C-peptid düzeyi) ve otoimmünite göstergeleri (otoantikorlar) tetkiki.
Kriterler tiplemede yetersiz kaldığında, spesifik diyabet tipleri düşünülerek dikkatli sorgulama ve ileri genetik analizler gerekecektir.
IV. DİYABETİN TEDAVİSİ
Tedavide amaç; gün içerisinde glisemik kontrolün sağlanması, akut komplikasyon gelişim riskinin azaltılması, mikrovasküler ve makrovasküler kronik komplikasyonların önlenmesi, eşlik eden diğer sorunların düzeltilmesi ve böylelikle diyabetlide yaşam kalitesinin yükseltilmesidir.
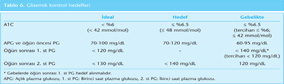
Halen geniş çapta kabul gören öneriler doğrultusunda erişkin diyabetliler için glisemik kontrol hedefleri Tablo 6’da gösterilmiştir.
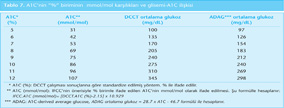
A1C değeri, ölçümden önceki ortalama üç aylık glukoz kontrolünü yansıtır. Testin yaptırılması için hastanın aç olması gereği yoktur. Yüksek performanslı likid kromatografi yöntemine göre normal sınırlar %4.0-6.0 arasındadır. A1C değerinin %50’si son bir ayda; %30’u ölçümden önceki ikinci ayda ve geri kalan %20’si ölçümden önceki üçüncü ayda oluşan glisemik değişiklikleri yansıtır. A1C değeri ne kadar normale yakınsa tokluk glisemisinin katkı payı ön plandadır; buna karşılık A1C arttıkça açlık glisemisinin katkısı daha çok artar. Son yıllarda IFCC, dünya genelinde A1C’nin halen kullanılmakta olan “%” yerine, “mmol/mol” birimiyle ifade edilmesini önermektedir. Alışılagelmiş “%” olarak ifade edilen A1C’nin “mmol/mol” karşılıkları Tablo 7’de gösterilmiştir. Buna göre A1C için ideal hedef olan %6.5’in yeni birim ile karşılığı 48 mmol/mol; kabul edilebilir hedef %7’nin karşılığı 53 mmol/mol ve nondiyabetik referans sınır %4.0-6.0’ın yeni birim ile karşılığı ise 20-42 mmol/mol’dür.
Diyabetlide tedaviye başlamadan önce hastanın vücut ağırlığı, boyu, BKİ, bel/kalça oranı (BKO) bilinmelidir. Tedavinin ana unsurları eğitim, tıbbi beslenme tedavisi, egzersiz ve medikal tedavidir.
1. EĞİTİM
Eğitim ile diyabetli bireye hastalığının ne olduğu, hangi belirti ve bulgularla seyredeceği; ideal tedavinin dayandığı esaslar ve uygulanması anlatılmalı; yetersiz tedavide gelişebilecek sorunlar ve önlenmesi ile ilişkili bilgilerle birlikte hastalıkla başedebilmenin yolları öğretilmelidir.
Diyabetli hasta öncelikle beslenme, egzersiz ve ilaç tedavisi üçgeni arasındaki dengeyi iyi kurabilmelidir. Sağlık ekibiyle diyaloğunu sürdürmeli, hangi şartlarda hastaneye başvurması gerektiğini bilmelidir.
Eğitimde esas olan evde kendi kendine glukoz ölçümünü yapabilmeyi sağlamaktır. Konuyla ilişkili TEMD’nin önerileri aşağıda sıralanmıştır:
1. İnsülin kullanan diyabetli bireylerde evde kendi kendine glukoz ölçümü diyabet öz-yönetiminin esas bileşenlerindendir.
2. Uluslararası otoriteler (örn. IFCC) tarafından onaylanmış ve plazma glukoz düzeylerine göre kalibre edilmiş glukoz ölçüm cihazları kullanılmalı, cihazın doğru ölçüm yaptığından emin olmak için en azından yılda bir kez ve ayrıca kuşkulu durumlarda açlık venöz plazma ile eş zamanlı ölçüm yapılmalıdır.
3. Tip 1 diyabetliler, gebe (gestasyonel diyabet veya pregestasyonel diyabet) diyabetliler ve bazal-bolus insülin tedavisi kullanan Tip 2 diyabetli hastalarda günde 3-4 kez öğün öncesi ve kişiye göre gerektiğinde öğünün ilk lokmasından iki saat sonrasında, ayrıca haftada bir gün gece yatarken ve ayda bir gün sabaha karşı saat 02.00-04.00 arasında glukoz düzeyi takip edilmelidir.
4. Yalnızca bazal insülinle birlikte oral antidiyabetik ilaç kullanan Tip 2 diyabetli hastalarda en azından günde bir kez ve değişik zamanlarda evde kendi kendine glukoz ölçümü yapılmalıdır.
5. Tıbbi beslenme tedavisi ve oral antidiyabetik ilaçlarla izlenen Tip 2 diyabetlilerde glisemik kontrol düzeyi, tedavi şekli ve kişisel özelliklere göre haftada 3-4 kez evde kendi kendine glukoz ölçümü önerilmelidir.
6. Gebelerde açlık ve birinci saat tokluk glukoz ölçümleri tercih edilmelidir.
7. Tedavi değişikliği yapılan dönemlerde, akut hastalık ve özel durumlarda ve ayrıca insülin pompası kullananlarda daha sık aralıklarla evde kendi kendine glukoz ölçümü yapılmalıdır.
2. EGZERSİZ
Tüm diyabetli hastalara, her hastanın özelliklerine uygun, komplikasyonlarına adapte edilerek planlanmış düzenli fizik aktivite önerilir. Egzersiz programı, genel sağlık yararları ve kilo kaybını kolaylaştırması bakımından önemlidir. Ancak egzersizin risklerini azaltmak için egzersiz öncesinden başlayarak egzersiz sırasında ve sonrasında emniyet ilkelerine dikkat edilmelidir.
Egzersiz öncesinde hastanın yaşına bakılmaksızın;
- Kronik komplikasyonların varlığı araştırılır.
- Glisemik kontrol düzeyi ve A1C gözden geçirilir.
- Kardiyak değerlendirme yapılır. Otuz beş yaşından büyük olanlara, yaşı 25’ten büyük olup diyabet süresi > 10 yıl olan Tip 2 veya > 15 yıl olan Tip 1 diyabetlilere, koroner arter hastalığı risk faktörleri bulunan diyabetlilere, periferik damar hastalığı, mikrovasküler hastalık veya otonom nöropatisi bulunanlara efor testi yapılmalıdır.
- Nörolojik ve kas-iskelet sistemi muayenesi, ayak muayenesi, fundus incelemesi yapıldıktan sonra kişiye özel ve uygun egzersiz belirlenir.
İdeal olan egzersiz; kişisel gereksinimler, sınırlamalar ve kişisel performansa göre bireyselleştirilen egzersizdir; program mümkünse bir egzersiz uzmanı tarafından, bireye uygun olarak düzenlenmeli ve başlangıçta uzman gözetimi altında yapılmalıdır.
- Günün hangi saatinde yapılacak egzersizin daha uygun olduğu konusunda görüş birliği yoktur; ancak egzersizin aç karnına veya yemekten hemen sonra yapılması sakıncalıdır. Hastanın koşulları belirleyici olmakla birlikte, akşam yemeğinden bir saat sonra yapılacak egzersizin Tip 2 diyabetlilerde sabah açlık plazma glukozu değerini düşürmede etkili olabileceği bilinmekte ve önerilmektedir.
- Egzersiz programı haftada en az üç gün olmalı ve egzersizler arasında iki günden fazla boşluk olmamalıdır.
- Diyabetlilerde daha ziyade aerobik egzersizler (tempolu yürüme, koşma, yüzme) tercih edilmelidir; dalış, yüksek irtifada yalnız uçma gibi sporlar önerilmemektedir.
Egzersiz süresince hastanın kalp hızını izlemesi ve maksimum kalp sayısının %60-75’ini aşmayacak bir hız ile egzersiz yapması önerilir. “Maksimum kalp hızı = 220-yaş” formülü ile hesaplanabilir.
- Hastanın diyabetli olduğunu belirtir bir takı (bilezik, kolye) kullanması veya kimlik kartı taşıması sağlanmalıdır.
- Egzersiz yaparken baş dönmesi, sendeleme, göğüste sıkıntı, dolgunluk, ağırlık, ciddi nefes darlığı ya da bulantı gelişirse egzersiz derhal sonlandırılmalıdır.
- Vücut aktivitesi ve ısısının artması insülin etkisini artırır, hipoglisemiye yol açabilir. O nedenle egzersiz boyunca kan glukoz düzeyini hızla yükseltebilecek karbonhidrat kaynağı yiyecek (glukoz tablet, kesme şeker, meyve suyu) bulundurmalıdır. Kan glukozu < 100 mg/dL ise egzersizden önce 15 g karbonhidrat alınması gerekir.
- Kan glukozu > 250 mg/dL ve keton (+) olan diyabetlinin egzersiz yapmasına izin verilmemelidir.
- Egzersiz öncesinde ve sonrasında ısınma ve soğuma egzersizleri ihmal edilmemelidir.
Egzersizin kontrendike olduğu haller; kan glukoz düzeylerinin ayarsız oluşu (glukoz ölçüm düzeyinin < 80 ve > 250 mg/dL), duysal polinöropati, proliferatif retinopati, kardiyovasküler hastalık ve hipoglisemiden haberdarsızlık (Hypoglycemia unawareness) mevcudiyetidir.
3. BESLENME DÜZENİ (Tıbbi Beslenme Tedavisi)
Tıbbi beslenme tedavisi, ADA tarafından, diyabet tedavisinin diğer yönleriyle beraber kalori alımının optimal koordinasyonunu tarif etmek için kullanılan bir terimdir. Hedefler biraz farklı olmakla birlikte, temel olarak, optimal tıbbi beslenme tedavisi bileşenleri, Tip 1 diyabetli ve Tip 2 diyabetli hastalarda aynıdır.
• Tıbbi beslenme tedavisinde amaç, glukoz düzeylerinin normale yakın düzeyde tutulmasını sağlamak, kardiyovasküler risk profilini azaltacak lipid profilini sağlamak ve kan basıncını normal veya normale yakın seviyede tutmaktır.
• Tıbbi beslenme tedavisi ile A1C düzeylerinde Tip 1 diyabette %1, Tip 2 diyabette %1-2; LDL-kolesterol düzeyinde %15-25 mg/dL azalma sağlandığı gösterilmiştir.
• Tıbbi beslenme tedavisi kişiye özel düzenlenmeli; planlamada hastanın beslenme alışkanlığı, boy, ağırlık, sosyoekonomik durumu bilinmelidir.
• Tip 1 ve Tip 2 diyabetli birey, tanıyı izleyen ilk ay, gestasyonel diyabetli birey ise tanıyla birlikte ilk hafta içinde mümkünse diyabet ekibindeki diyetisyen tarafından değerlendirilmelidir.
• Basılı diyet listelerinin geçerliliği, güvenilirliği yoktur.
• Tıbbi beslenme tedavisi uygulanırken dört temel basamak göz önünde bulundurulmalıdır. Öncelikle hastanın antropometrik ölçümleri, sosyal yaşam anamnezi, kendi koşullarındaki beslenme durumunun değerlendirilmesi gerekir. Bu bilgiler ışığında saptanan uygun enerji ve makronütrient tüketim düzeyi saptanır. Ulaşılabilir ve uygulanabilir spesifik davranış biçimi hastayla birlikte belirlenerek mevcut sorunların çözümüne odaklanması sağlanır.
Başlıca karbonhidrat, protein ve yağ olarak gruplanan makronütrient besin ögelerinin bir diyabetlide kullanımında aşağıda açıklanan hususlara dikkat etmek gerekir.
Diyabet Tedavisinde Karbonhidrat
• Sağlıklı olmak için gerekli beslenme modeli, tam taneli tahıllar, meyveler, sebzeler ve düşük yağlı süt gibi karbonhidratlı besinleri içermelidir.
• Diyabet tedavisinde, günlük karbonhidrat alımını 130 g’ın altında tutan düşük karbonhidratlı diyetler önerilmez. Önerilen, günlük besin kapsamında karbonhidrat oranının %60-70 olmasıdır.
• Karbonhidrat sayımı, değişim listeleri veya deneyime dayalı hesaplama yoluyla karbonhidrat alımının izlenmesi, glisemik kontrolün sağlanmasında kilit noktadır.
• Alınan günlük toplam karbonhidrat miktarı yanında, karbonhidratların glisemik indeks ve glisemik yükünün dikkate alınması glisemik kontrolde ek yarar sağlayabilir.
• Sukroz içeren besinler, öğün planı içinde karbonhidrat miktarı denk bir besinin yerine kullanılabilir, eğer öğün planına bir yer değiştirme olmadan ilave edilirse insülin veya oral antidiyabetik ilaç dozu ayarlanmalıdır. Sukroz ve sukroz içeren besinler sağlıklı diyet kapsamında 30 g/gün miktarında tüketilebilir. Aşırı enerji alımından sakınılması gerektiği de unutulmamalıdır.
• Posa tüketimi desteklenmelidir, ancak diyabetli bireylere genel popülasyona önerilen miktarlardan daha fazla miktarlarda posa tüketimi önermek gerekmez. 20-35 g/gün posa tüketimi yeterlidir.
Diyabet Tedavisinde Yağ ve Kolesterol
• Doymuş yağ alımı toplam kalorinin %7’sinden az olacak şekilde sınırlandırılmalıdır.
• Trans yağ alımı çok azaltılmalıdır.
• Diyabetli bireylerde kolesterol alımı günde 200 mg’ın altında olmalıdır.
• Haftada iki veya daha fazla porsiyon balık, omega-3 çoklu doymamış yağ asitleri sağlar ve bu miktarda tüketim önerilmelidir.
Diyabet Tedavisinde Protein
• Genel toplumda günlük enerjinin %15-20’sinin proteinlerden karşılanması önerilmektedir. Renal fonksiyonlar normalse diyabetli bireylerde bu öneriyi modifiye etmeye gerek yoktur.
• Tip 2 diyabetli bireylerde proteinlerin sindirimi kan glukoz konsantrasyonunu artırmaksızın insülin yanıtını artırabilir. Bu nedenle proteinler akut hipoglisemide veya gece hipoglisemilerinin tedavisinde kullanılmamalıdır.
• Ağırlık kaybını sağlamak için yüksek proteinli diyetler önerilmez. Enerjinin %20’sinden fazla protein alımının diyabet tedavisi ve komplikasyonları üzerine etkisi bilinmemektedir. Bu tip diyetler kısa dönemde ağırlık kaybı sağlayabilir ve glisemiyi iyileştirebilir. Ancak bu faydaların uzun dönemde de sağlandığı saptanmamıştır.
Diyabet Tedavisinde Yapay Tatlandırıcıların Yeri
1. Enerji değeri azaltılmış tatlandırıcılar (şeker alkolleri; poliyoller): Eritritol, izomalt, laktilol, maltilol, sorbitol, mannitol, ksilitol, tagatoz ve hidrojenize nişasta hidrolizatları kalorisi azaltılmış (enerji değerleri 0.2-3.0 kcal/g arasında değişen), “Food and Drug Administration (FDA)” tarafından onaylanmış tatlandırıcılardır.
2. Enerji içermeyen tatlandırıcılar: Asesulfam K, aspartam, neotam, sakkarin ve sukraloz enerji içermeyen (besleyici olmayan) tatlandırıcıların 70 kg’lık bir erişkine, FDA tarafından önerilen maksimum günlük miktarları sakarin ve siklamat için 8 tablet/gün, aspartam için 19 tablet/gün ve asesulfam-K için 175 tablet/gündür.
Yapay tatlandırıcıların obez ve kilolu kişilerde kilo kaybını sağlamak ve diyabeti önlemek amacıyla kullanım endikasyonları bulunmamaktadır. Fruktoz içeren tatlandırıcıların fazla miktarda kullanılması hipertrigliseridemiye neden olabilir; mannitol ve sorbitol gibi tatlandırıcı grubu ishale yol açabilir; aspartam kullanımında fenilketonürili bireylerde hastalık alevlenebilir.
Diyabet Tedavisinde Alkol
• Diyabetli bireylerin alkol kullanması önerilmez. Alkol alımı glisemik kontrolü bozuk, hipoglisemi riski yüksek veya ketozu olan ya da akut kardiyovasküler olay, kontrolsüz hiperlipidemi, pankreatit, karaciğer yağlanması gibi sorunları bulunanlarda ciddi sağlık sorunlarına yol açabilir.
• Yukarıda bahsedilen riskleri olmayan diyabetli bir yetişkin alkol kullanmayı tercih ediyorsa, haftada iki günü geçmemesi koşuluyla, önerilen günlük alım miktarı kadınlar için 1 birim, erkekler için 2 birimdir. Bir birim alkol, 7.9 g saf etanol olarak tanımlanmaktadır; ancak alkolün sıvı ve hacimle ölçülmesi daha kolay olması nedeniyle “bir birim alkol” 10 mL alkol demektir. Bu oran kabaca yarım bardak bira, elma şarabı; 25 mL votka, viski ya da cin; 50 mL Porto ya da İspanyol şarabı veya 125 mL şarap örneklerine denk gelmektedir.
Diyabet Tedavisinde Diyet Ürünleri
Gereksizdir.
Diyabetlide Tuz
Genel popülasyona önerildiği gibi doz < 3000 mg/gün olmalıdır.
Diyabet Tedavisinde Mikronütrientler
Yetersizlik belirtisi olmadığı sürece vitamin ya da mineral takviyesine gerek yoktur. Uzun dönemli kullanımında güvenilir ve etkinliği yönünde yeterli kanıt gösterilemediğinden C, E ve karoten antioksidanların rutin kullanımı önerilmez. Krom takviyesinin faydaları açıkça kanıtlanmamıştır.
Öğün Planlamasında Hangi Yöntemler Kullanılmalıdır?
Öncelikle bireyin yaşam tarzı, eğitim düzeyi ve uygulama becerisi göz önüne alınarak planlama yapılmalıdır. Başlıca yöntemler “tabak modeli” ve “karbonhidrat sayım tekniği”dir.
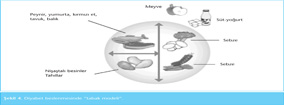
Şekil 4’te gösterilen “Tabak yöntemi” sağlıklı beslenme prensiplerinin anlatılmasında, karbonhidrat alımının sınırlandırılmasında görsel olarak kullanılan ve kısa sürede bilgi vermeyi sağlayan bir yöntemdir. Ev dışında yemek yeme alışkanlığı fazla olan, eğitim düzeyi düşük ve besin tüketiminde karbonhidrat, protein alımı yüksek olan bireylerde kullanılabilir.
“Karbonhidrat sayım tekniği” daha iyi glisemik kontrol sağlanabilmesi için öğünlerde tüketilecek karbonhidrat oranının ayarlanmasına, tüketilecek karbonhidrat miktarına uygun insülin dozu uygulanmasına veya öğün öncesi şeker düzeyine göre insülin dozunun ayarlanmasına olanak sağlayan bir öğün planlama yöntemidir. Bu yöntemin birinci düzeyinde diyabetli bireye 15 g karbonhidrat içeren besin grupları ile günlük yaşamında tüketeceği besinlerin porsiyon ölçülerine göre aldığı karbonhidrat miktarı anlatılır (Tablo 8). Glisemi kontrolü sağlanmış ve bazal insülin dozu iyi ayarlanmış bireyde ileri düzey karbonhidrat sayımı eğitimine geçilebilir. Bu düzeydeki eğitimde özellikle insülin pompası ve çoklu insülin kullanan diyabetliye “karbonhidrat/insülin oranı (KH/İ) ve “insülin duyarlılık faktörü (İDF)” hesaplanması öğretilir.
“KH/İ= 500/Günlük toplam insülin dozu”, “İDF= 1500/Günlük toplam insülin dozu” formülleriyle hesaplanır. Analog insülin kullanıyorsa formül: “İDF= 1800/Günlük toplam insülin dozu” olarak değiştirilir.
Tip 1 diyabet (özellikle pompa kullananlarda), gestasyonel diyabet tanısı alan ya da diyabet riski olan ve hatta reaktif hipoglisemili bireyler için yararlı bir yöntemdir. Karbonhidrat sayımı öğretilen bireye protein ve yağ tüketiminin de önemli olduğu mutlaka anlatılmalıdır.
4. MEDİKAL TEDAVİ
Tedavide ilk basamaktan itibaren her aşamada, egzersiz ve vücut ağırlığının normale gelmesini sağlayan tıbbi beslenme tedavisi ve egzersizden ibaret yaşam tarzı değişikliği ön planda ele alınmalıdır. Ancak, Tip 2 diyabette uzun vadede bu önlemler metabolik kontrolü sağlamada yetersiz kaldığı için hastaların çoğu kısa sürede en azından ağızdan kullanılan bir ilaçla tedaviye ihtiyaç duymaktadır. Tip 1 diyabette ise yaşamın sürdürülmesi insülin tedavisiyle mümkün hale gelmiştir.
Medikal tedavi, oral antidiyabetik ilaçlar ve insülin olarak gruplanır.
ORAL ANTİDİYABETİK İLAÇLAR
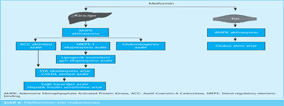
Şekil 5’te fizyopatolojik etki mekanizmaları gösterilen oral antidiyabetik ilaçlar dört gruptur. Etkinliklerini karaciğer, kas, yağ dokusu ve bağırsaklar üzerinden gösterir.
A. Karbonhidrat emilimini azaltanlar; α-glukozidaz inhibitörleri,
B. İnsülin duyarlılığını artıran ilaçlar; metformin, tiazolidinedionlar,
C. İnsülin sekresyonunu artıran ilaçlar; sülfonilüreler, meglitinid analogları,
D. İnkretin bazlı tedaviler; gliptinler: Glukagon-likepeptid-1 reseptör agonistleri (GLP-1RA) ve dipeptidil Peptidaz-4 inhibitörleri (DPP-4 Inh).
A. KARBONHİDRAT EMİLİMİNİ İNHİBE EDEN İLAÇLAR
α-glukozidaz İnhibitörleri
Besinlerle aldığımız kompleks karbonhidratlar, ince bağırsak lümeninde pankreastan salgınan a-amilaz ve ince bağırsaklardan salgılanan α-glukozidaz enzimleri sayesinde parçalanarak oligosakkaride dönüşür ve emilir. Adı geçen enzimlerin inhibe edilmesiyle kompleks karbonhidratların emilimi geciktirilirse, karbonhidratların emilimi daha distale ve kolona kayarak ikinci saat plazma glukozu düzeyini yavaşlatır. Bu amaçla geliştirilmiş olan α-glukozidaz inhibitörleri sülfonilüre ve metformine göre nispeten yeni geliştiren, diğer oral antidiyabetik ilaçlara oranla da rölatif olarak daha zayıf etkili antihiperglisemik ilaçlardır. Bu grubun üyeleri akarboz, vogliboz ve miglitoldür. Ülkemizde yalnızca nitrojen içeren psödotetrasakkarid yapısındaki akarboz piyasada bulunmaktadır (Tablo 9).
Etki mekanizması: α-glukozidaz inhibitörleri, karbonhidratlarla yarışarak ince bağırsak epitelinde fırçamsı membrana bağlı bulunan maltaz, izomaltaz, sukraz, glukoamilaz gibi disakkaridazları 4-6 saat süreyle bloke eder. 10-100.000 kat daha fazla bir afiniteyle sağladıkları inhibisyon sayesinde karbonhidrat emilimi gecikir ve ikinci saat plazma glukozu pik düzeyi azalır. Akarboz, grubun ilk keşfedilen üyesidir, glukoamilaz, maltaz, sukroz, dekstranaz, pankreatik amilaz üzerine etkilidir. İzomaltaz üzerine etkisi azdır, laktaz enzimi ve glukoz taşıyıcılar üzerine etkisi olmadığından dolayı karbonhidrat emilimini geciktirse de glukozun tamamının emilmesini engelleyemez. Yaklaşık %2’si sistemik dolaşıma geçer, çoğu dışkı ile atılır. Günlük dozu 25-300 mg olup, ana yemeklerle birlikte veya tok karnına, az miktarda su ile yutulması önerilir; yan etkilerin ortaya çıkışını engellemek için günde 1-3 kez 25 mg ile başlanır, tedricen 1-2 hafta aralarla artırılarak, 3 x 100 mg dozuna çıkılabilir. Asetheksamid, alatrofoksasin, klorpropamid, siprofloksin, klinafloksasin, gemifloksasin, glipizid, gliburid, levofloksasin, norfloksasin, ofloksasin, tolazamid gibi ilaçlarla etkileşime girebilir.
Etkinliği: α-glukozidaz inhibitörleri monoterapide kullanılacağı gibi insülin, sülfonilüre, metformin, tiazolidinedion, glitazon gibi pek çok ilaç ile kombinasyon tedavisinde kullanılabilir. Birçok çalışmada APG’yi 25-30 mg/dL, tokluk glukozunu 40-50 mg/dL; A1C değerlerini %0.5-1.0 oranında düşürdüğü gösterilmiştir. Monoterapideki etkinliği metformin ve sülfonilüreden daha azdır. Kilo aldırmadan glisemik kontrolü sağlayabilir, genellikle hipoglisemiye yol açmaz. Tip 2 diyabetlilerde akut dönemde gastrointestinal insülinotropik peptid (GIP) düzeyini azalttığı, GLP-1 düzeyini ise artırdığı gösterilmiştir. Böylelikle mide boşalımını da geciktirdiği ve kilo kaybını sağladığı gösterilmiştir. Nondiyabetiklerde vücut ağırlığına etkili değildir.
Bekleneceği gibi etkilerinin büyük kısmı ikinci saat plazma glukozu üzerinedir; açlık glukozuna çok az etkileri vardır. Postprandiyal hipergliseminin kardiyovasküler mortaliteyi artırdığı ispatlandıktan itibaren akarboza ilgi artmış ve etkinliği çok sayıda çalışmada araştırılmıştır. “The Study to Prevent Non-Insulin Dependent Diabetes Mellitus (STOP-NIDDM)” çalışmasında akarbozun kardiyovasküler olay riskini %4.7’den %2.1 düzeyine azalttığı gösterilmiştir (HR: 0.51, %95 GA, 0.28-0.95). “The Meta-Analysis of Risk Improvement under Acarbose (MeRIA)” çalışmasında tüm kardiyovasküler olaylarda %35, miyokard infarktüsü riskinde %64 azalma bildirilmiştir (HR= 0.36, %95 GA, 0.16-0.80; p= 0.012). IGT’li bireylerde ikinci saat plazma glukozu düzeyinde hızlı yükselmenin endotel hasarına ve proaterojenik olayların başlamasına yol açması göz önünde tutularak, prediyabetik bireylerde akarbozun aterosklerozdaki etkinliği araştırılmış; STOP-NIDDM çalışmasının bir alt grubu olan çalışmada IGT’li bireylerde intima-media kalınlığındaki progresif artışın akarboz tedavisi ile yavaşladığı gösterilmiştir. Akarbozun diyabet prevansiyonunda yeri olup olmadığı açısından planlanan STOP-NIDDM çalışmasında akarboz tedavisi ile Tip 2 diyabete dönüşün %32 azaltılabileceği gösterilmiştir. Otuz dokuz aylık izlem süresince diyabet insidansı plasebo grubunda %42 iken, akarboz grubunda %32 bulunmuştur (RR: 0.75, %95 GA 0.63-0.90).
Yan etkileri: Akarbozun güvenilirliğini araştırmak amacıyla planlanan 6000 hasta üzerinde, 28 haftalık “Precose Resolution of Optimal Titration to Enhanca Current Therapies (PROTECT)” çalışmasında güvenli ilacın olduğu gözlemlenmiştir.
• Akarbozun majör yan etkisi gastrointestinal sistem (GİS) ile ilişkilidir. Absorpsiyona uğramamış karbonhidratlar kolondaki bakteriler tarafından metabolize edilerek emilir. Bu esnada açığa çıkan yağ asidi, metan, hidrojen ve CO2 ishal, şişkinlik (meteorizm), karın ağrısı gibi GİS semptomlarına yol açar. Bu yan etkiler hastaların %25’inde gözlenir. Dozu minimalden başlayarak ve doz titrasyonu yaparak semptomlar azaltılabilir. İlacın devam edilmesiyle yan etkilerin dört hafta içinde azalabildiği görülmüştür. Bunun muhtemel sebebi, ince bağırsağın distal kısmında artan enzim aktivitesine bağlı olarak GLP-1 salınım miktarı ya da etkinlik süresinin artmasıdır.
• Nadiren demir eksikliğine yol açabilir.
• Monoterapide kullanıldığında çoğu kez hipoglisemiye yol açmamakla birlikte alkolle birlikte alındığında ya da sülfonilüre preparatları, insülin ya da MGA ile kombine edildiğinde de hipoglisemiye yol açabileceği unutulmamalıdır. Akarboz hipoglisemisinde sakarozun ve glukagon enjeksiyonunun etkisi yoktur, saf glukoz, dekstroz ya da süt ile tedavi edilir.
• Nadiren idiyosenkrazi ya da doza bağlı hepatotoksisite görülebilir. Yüksek doz, örneğin; günde 3 x 200 mg’ın üzerinde kullanıldığında karaciğer enzimlerinin yükseldiği gösterilmiştir. Muhtemel sebebi molekülün kendisi ya da metaboliti olan 4-metilpirogallol derivelerine karşı gelişen idiyosenkrazik reaksiyondur.
Kontrendikasyonları: İnflamatuvar bağırsak hastalıkları, peptik ülser, malabsorpsiyon, karaciğer sirozu, intestinal obstrüksiyon, akut böbrek yetmezliği kreatinin düzeyi > 2 mg/dL ya da glomerüler filtrasyon oranı (GFR) < 25 mL/dakika olan hastalarda kontrendikedir.
Gebelikte, laktasyon döneminde ve 12 yaş altı çocuklarda güvenli kullanımı için yeterli veri olmaması nedeniyle kullanılması önerilmez.
Özetle α-glukozidaz inhibitörleri, karbonhidratlarla yarışarak ince bağırsak epitelinde fırçamsı membrana bağlı bulunan disakkaridazları bloke ederek, sağladıkları inhibisyon sayesinde karbonhidrat emilimini geciktiren ve ikinci saat plazma glukozu pik düzeyini azaltan ilaçlardır. Metformin kullanılamayan Tip 2 diyabetlilerde monoterapide kullanılacağı gibi kontrendikasyonu olmayan Tip 2 diyabetlilerde insülin, sülfonilüre, metformin, tiazolidinedion, glitazon gibi pek çok ilaç ile kombinasyon tedavisinde kullanılabilir. Sistemik dolaşıma girmez, majör yan etkisi GİS ile ilişkilidir. İnflamatuvar bağırsak hastalığı, karaciğer sirozu, akut böbrek yetmezliği olanlarda gebelik ve çocukluk döneminde kullanılmamalıdır.
B. İNSÜLİN DUYARLILIĞINI ARTIRAN (SENSİTİZER) İLAÇLAR
Bu grupta biguanidler ve tiazolidinedionlar (glitazonlar) olmak üzere iki alt grup ilaç yer alır (Tablo 10). Biguanidler karaciğer düzeyinde, glitazonlar ise daha ziyade yağ dokusu düzeyinde insülin duyarlılığını artırıcı etki gösterir.
Biguanidler
Biguanid türevlerinin diyabet tedavisindeki kullanımı çok eskilere dayanır. Galega officinalis (Fransız Leylağı) adı verilen bitkiden elde edilen bir guanidin türevidir. Diğer guanidin türevlerinden sintalin-A 1920’li yıllarda kullanılmış, hepatotoksisite nedeniyle kullanımdan kaldırılmıştır; fenformin ise 1960-1970’li yıllarda Amerika Birleşik Devletleri (ABD)’nde yoğun kullanılmış, laktik asidoz nedeniyle piyasadan çekilmiştir; o yıllarda başka bir guanidin türevi buformin olarak Almanya’da kullanılmıştır. Metformin ise Avrupa ülkelerinin çoğunda o yıllardan itibaren kullanımda iken, ABD’de 1995 yılında yeniden piyasaya sürülmüştür.
Metformin
İnsülin direncini hem kas hem de karaciğer düzeyinde azaltmakla birlikte, etkinliği daha ziyade karaciğer düzeyindeki insülin direncini iyileştirme yönündedir.
Etki mekanizması: Şekil 6’da özetlenmiştir. Metformin, temel olarak karaciğerde glukoneogenezi ve az da olsa glikojenolizi baskılamak suretiyle hepatik glukoz üretimini azaltır. Bu etki muhtemelen bir intraselüler enerji sensörü olan ve glukoneogenez üzerinde kritik bir rolü bulunan AMPK (Adenosine Monophosphate Activated Protein Kinase) aracılığıyla gerçekleşmektedir. AMPK’yi fosforilleyerek aktive edilmesini sağlayan ise bir tireonin kinaz proteini olan LKB1’dir. Bu bilgi, LKB1 delesyonu yapıldığında glukoneogenezin ve lipogenik enzimlerin gen ekspresyonunun arttığının görülmesi ve metforminin glukoz düşürücü etkisinin ortadan kalktığının saptanmasıyla kanıtlanmıştır. AMPK karaciğer ve kas dokusunda aktive olarak glukoz ve lipid metabolizmasında olumlu etkilere neden olur. Karaciğerde aktive olduğunda hepatik glukoneogenezde önemli rol oynayan PEPCK (fosfoenol karboksi) ve glukoz-6-fosfataz enzimlerinin gen ekspresyonları inhibe olur; ayrıca karaciğerde yağ asidi sentezini artıran ACC (Acetyl-CoA carboxylase) ve SREPB-1 (Sterol-Regulatory-Element-Binding) enzimlerini baskılayarak yağ asidi sentezini azaltır. Böylelikle karaciğerde yağ depolanmasını ve kana trigliserid, VLDL-kolesterol, LDL-kolesterol taşınmasını azaltır. AMPK ayrıca iskelet kasında ve yağ dokusunda glukozu hücreye taşıyan GLUT-4 ekspresyonunu artırarak glukoz utilizasyonunu artırır. GLUT-1 düzeyine de etkili olduğu gösterilmiştir. Metformin pankreas beta-hücreleri üzerine direkt etkili değildir. Ancak insülin duyarlılığını artırarak oluşturduğu antihiperglisemik etkinliği sonucu glukotoksisiteyi azaltarak indirekt etkiyle beta-hücre fonksiyonlarını iyileştirici etkileri gözlenmiştir. İnce bağırsaktaki L hücrelerinden GLP-1 sekresyonunu artırdığı iddia edilmektedir; böylelikle dolaşımdaki GLP-1 düzeylerini artırarak varolan metabolik etkileri güçlenmektedir. Dipeptidil peptidaz-4 (DPP-4) enzimi üzerinde bir etkisi gösterilememiştir. Metforminin etki mekanizmalarından bir diğeri de intestinal glukoz absorpsiyonunu azaltmasıdır.
Etkinliği: Metforminin glukoz düşürücü etki potansiyeli esas olarak sülfonilürelerle aynıdır, plaseboya göre A1C düzeyinde %1-2 düşüş sağlar. Biyoyararlılığı %50-60 kadardır. Esas olarak ince bağırsaklardan absorbe edilir, 1-2 saat içinde pik yapar; etki süresi 5-6 saattir. Pratik anlamda plazma proteinlerine bağlanmaz, tüm dokularda plazmadaki konsantrasyonuna yakın olarak dağılır. Alınmasından 12 saat sonra glomerüler filtrasyon ya da tübüler sekresyon yoluyla böbreklerde %90 elimine edilir. Etkisinin başlaması hızlı değildir. Tedavinin başlanmasından sonraki 2-3 gün içinde kan glukozunu düşürücü etkisi belirmeye başlar, iki haftada pik etkisine ulaşır. Monoterapi olarak kullanıldığında etki mekanizmasından dolayı hipoglisemiye neden olmaz, bu açıdan sekretogoglardan avantajlıdır. Hipoglisemiye yol açmamasının sebebi, glukoneogenez için önemli bir ön ürün olan laktatın yapımındaki artışa yanıt olarak insülin sekresyonunun yeterli olmayışıdır. Böylelikle laktatın glukoza dönüşümüyle artmış olan hepatik glukoz çıkışı ile hipoglisemi önlenmiş olur. Üstelik anorektik etkisi nedeniyle vücut ağırlığında azalmaya veya en azından kilonun nötr kalmasına neden olması da bir avantajdır. Monoterapide metforminin etkinliği α-glukozidaz ve DPP-4 inhibitörlerinden daha fazladır, tiazolidinedion ile karşılaştırıldığında etki gücünün eşit ve tiazolidinedion etki mekanizmasını tamamlayıcı bir rolü olduğu söylenebilir.
Metforminin glukoz düşürücü etkileri yanında diğer faydaları da gösterilmiştir (Tablo 11). Bunlar arasında kardiyovasküler sisteme, lipid düzeylerine, adipoz dokuya olumlu etkileri sayılabilir.
Kardiyovasküler sisteme etkileri: Yapılan pek çok çalışmada metforminin kardiyovasküler koruyucu etkisi gösterilmiştir. Yeni tanı alan Tip 2 diyabetli hastaların ortalama 11 yıl izlendiği UKPDS çalışmasında metformin kullananlarda tüm nedenlere bağlı mortalite, diyabetle ilişkili mortalite, miyokard infarktüsü ve diyabete bağlı komplikasyonlar daha az görülmüştür. Çalışmada metformin alan hastalar, konvansiyonel (yalnızca diyet) tedavi alanlarla karşılaştırıldığında glisemi kontrolünün göstergesi A1C, metformin grubunda %7.4 iken, yalnızca diyet yapan grupta %8 olarak saptanmıştır. A1C düzeyinde 0.6’lık bir azalma beraberinde önemli sonuçlar doğurmuştur. UKPDS çalışmasının sonuçlarını şöyle özetleyebiliriz:
a. Metformin kullanan grupta, mikro ve makrovasküler komplikasyonlar %31 oranında daha azdır.
b. Metformin alanlarda, yaşam süresi daha uzun bulunmuştur. Metformin diyabetle ilişkili mortaliteyi %42, tüm nedenlere bağlı mortaliteyi %36 azaltmıştır.
c. Metformin, miyokard infarktüsü ve kalp hastalığına bağlı mortaliteyi azaltmıştır. Bu azalma, çalışmanın bitirildiği tarihte istatistiksel anlamlı bulunmamışken; çalışmanın tamamlanmasından 10 yıl sonrasında aynı hastalar yeniden değerlendirildiğinde, hastalığın erken döneminde iyi glisemi kontrol sağlanan gruptaki bireylerde makrovasküler komplikasyon gelişimi ve mortalitenin daha az ve istatistiksel anlamlı olduğu gösterilmiştir. Bu bilgi “metabolik hafıza” teorisini ortaya koymuş; tedavide erken, intensif yaklaşımın önemini göstermiştir.
“Prevention of Restenosis with Transilast and its Outcomes (PRESTO)” çalışmasında metformin kullananlarda, kullanmayanlara oranla kardiyovasküler herhangi bir olay, miyokard infarktüsü tüm nedenlere bağlı mortalite ve revaskülarizasyona bağlı iskemi üzerinde olumlu etkiler gösterilmiştir.
Lipid düzeylerine etkisi: Etki mekanizmasında açıklandığı üzere metforminin lipid profiline olumlu etkileri pek çok klinik çalışmada gösterilmiştir. Başlıca etkileri total kolesterol, LDL-kolesterol ve VLDL-kolesterol düzeylerinde azalma şeklinde görülmektedir. Bunun yanında HDL düzeylerinde azalma gözlenmemiştir.
Adipoz doku üzerine etkisi: Metforminin kullanımıyla kilo kaybı görülmektedir. Bunun iştah merkezine olan direkt etkisinin yanı sıra glukozun bağırsaktan emilimini azaltmasına da bağlamak mümkündür. Tedavinin ilk altı ayında vücut ağırlığında 2.5-4.5 kg’lık bir azalma sağlanabilir.
Hemostaz üzerine etkisi: Yapılan randomize kontrollü klinik çalışmalarda plazminojen aktivatör inhibitör-1 (PAI-1) düzeylerini azalttığı, doku plazminojen aktivatör (tPA) düzeylerini artırdığı gösterilmiştir. Dolayısıyla fibrinoliz ve periferik dolaşım üzerine olumlu etkileri vardır. Ayrıca, trombosit agregasyonunun azalttığı, pıhtılaşma faktörlerinden FVII ile trombosit formasyonu ve stabilizasyonundan sorumlu FXIII aktivitesini azalttığı gösterilmiştir.
Antiaterosklerotik etki: Metforminin vasküler endotelden salınan adezyon moleküllerinin (ICAM-1, VCAM-1, E-selektin) ekspresyonunu inhibe ettiği, oksidatif stresi azalttığı, mikrosirkülasyonu artırarak kan akımını hızlandırdığı gösterilmiştir.
Potansiyel klinik etkinliği: Prospektüse giren kesin kullanım endikasyonu olmamakla birlikte metforminin diyabetin önlenmesi, polikistik ve nonalkolik hepatosteatoz (NASH)’da kullanımı, kanser önleme konularında etkinliği gündemdedir.
• Diyabet önleyici rolüne ait bulgular ABD’de yapılmış olan DPP (Diabetes Prevention Program) çalışmasına dayanmaktadır. Bu çalışmada bozulmuş glukoz toleransı olan (IFG ve/veya IGT) prediyabetli bireylerde yaşam tarzı değişikliğinin, yaşam tarzı değişikliği + metformin grubuyla karşılaştırıldığında metformin ile diyabet risk azalmasının %31 daha az olduğu gösterilmiştir.
• Polikistik over sendromu, insülin direnci ile olan ilişkisi gösterildiğinden beri metformin ovülasyon indüksiyonu için kullanılmakta olan klomifene ek olarak ya da monoterapide kullanım endikasyonu bulmuş; üstelik polikistik over sendromlu insülin direnci olan hastalarda ovülatuvar fonksiyonları da düzelttiği ve güvenilirliği yapılan çalışmalarla kanıtlanmıştır.
• İnsülin direncinin eşlik ettiği nonalkolik karaciğer yağlanması (NASH) ve HIV infeksiyonlarında metforminin yararlı olduğunu gösteren çalışmalar mevcuttur.
• Metforminin AMPK enzimini aktive ederek etki ettiğini, AMPK regülatörünün de LKB1 olduğunu önceki bölümlerde ifade etmiştik. LKB1’in tümör süpresör etkisi vardır; bu yolağın metformin ile aktif hale geçişi antitümör etkinlik yaratabilir. İki gözlemsel çalışmada diğer tedavilerle kıyaslandığında metformin alanlarda kanser riski daha az bulunmuştur.
Yan etkileri: En sık görülen yan etkisi %5-20 oranında GİS yan etkileri olup, ağızda metalik tat, anoreksi, bulantı, kusma, midede yanma, kramp, şişkinlik hissi ve ishal şeklinde ortaya çıkabilir. İlaç dozunun yavaşça titrasyonu ile bu risk azaltılabilir. GİS intoleransı sıklıkla tedavinin üçüncü haftasında geçebilmektedir. 2550 mg/gün dozuna kadar çıkarılabilse de optimal günlük doz 2000 mg’dır. Laktik asidoz çok nadir bir komplikasyondur, her 30.000 hasta-yıl kullanım için bir kez olduğu bildirilmiştir. Bu yan etki tipik olarak böbrek yetmezliği veya diğer bazı hemodinamik bozukluğu olan hastalarda görülür. Bazı aşırı duyarlı kişilerde hafif eritem bildirilmiştir. Uzun süreli metformin kullananlarda homosistein ve B12 emilimini azalttığı, ancak bunun klinik anlamı olmadığı bildirilmektedir.
Kontrendikasyonları: Bugün için monoterapi veya sülfonilüre, glinid, tiazolidinedion veya insülinle birlikte kombinasyon tedavisinde kullanımı onaylanmıştır. Böbrek yetmezliği (serum kreatinin değerinin erkekte 1.5 mg/dL’nin, kadında 1.4 mg/dL’nin üzerinde olduğu durumlar ya da GFR < 60 mL/dakika olması hali), kalp yetmezliği, kronik karaciğer hastalığı (karaciğer enzimlerinin normal değerin ≥ 3 katı olması durumu), metabolik asidoz, dehidrasyon, kronik alkolizm, akut alkol intoksikasyonu veya hemodinamik durumu bozuk, hipoksi (akut miyokard infarktüsü, kardiyak yetersizlik, pulmoner yetersizlik, sepsis, şok) tablosunda olan hastalarda kullanılmamalıdır. Tedavi başlarken böbrek fonksiyonları kontrol edilmeli; perioperatif koşullarda veya kontrastlı radyolojik tetkikten 48 saat öncesinde kesilmelidir. Seksen yaşın üzerindeki hastalarda dikkatli kullanılmalıdır, ancak genel durumu iyi olanlarda, düşük doz tercih edilerek böbrek fonksiyonları değerlendirildikten sonra kullanılabilir.
Özetle metformin, GİS’ten glukoz girişini sınırlar, hepatik glukoz çıkışını baskılar, periferik dokularda insülinin işlevini potansiyalize ederek glukozun kullanımını artırır. Bu metabolik etkisinin yanı sıra vasküloprotektif etki ve lipid profiline olumlu etkisi olması ve kilo kaybını stimüle etmesi nedeniyle; günümüzde ADA, EASD ve IDF tarafından yapılan tedavi algoritmalarında Tip 2 diyabet tedavisinde yaşam tarzı değişiklikleri yanında ilk tedavi seçeneği (tedavinin lokomotifi) olarak önerilmektedir. Metformin, yeni başlangıçlı Tip 2 diyabetlilerde yaşam tarzı değişiklik önerisiyle birlikte ilk seçenek olarak monoterapi biçiminde önerilmektedir; maksimum dozda diğer seçenekler kullanıldığı halde kontrolsüz olan diyabetlilerde diğer ilaçlarla kombinasyon tedavisinde kullanılabilir. Bugün için monoterapi veya sülfonilüre, glinid, tiazolidinedion veya insülinle birlikte kombinasyon tedavisinde kullanımı onaylanmıştır. Önemli yan etkileri, ağızda metalik tat, anoreksi, bulantı, kusma, midede yanma, kramp, şişkinlik hissi ve ishaldir. Uzun kullanımlarda B12 eksikliğine yol açabilir. Böbrek yetmezliği, kalp yetmezliği, kronik karaciğer hastalığı, metabolik asidoz, dehidrasyon, kronik alkolizm, akut alkol intoksikasyonu veya hemodinamik durumu bozuk, hipoksi tablosu olan hastalarda kontrendikedir.
Tiazolidinedionlar = Glitazonlar
Tiazolidinedionlar son yıllarda tartışılır hale gelmiş olmalarına rağmen, insülin direncini azaltarak kan şekerini düşüren orijinal antidiyabetik ilaçlardır. İlk kez 1970’li yıllarda keşfedilmiştir. Grubun ilk üyesi troglitazon 1997 yılında kullanıma girmiş, 2000 yılında ciddi hepatotoksisitesi nedeniyle piyasadan çekilmiştir. Grubun iki üyesi; rosiglitazon ve pioglitazon 1999 yılında onay almışlardır. 2007 yılında Niessen ve Wolski, rosiglitazon ile yapılan kısa süreli 42 çalışmanın meta-analizine dayanarak rosiglitazon kullanımının miyokard infarktüsü riskiyle ilişkili olduğunu ve kardiyovasküler mortaliteyi artırdığını bildirmişlerdir. Konu FDA tarafından değerlendirilmiş ve FDA iddianın dayandırıldığı çalışmaların çoğunun kardiyovasküler olayları araştırmak için planlanmadığını ve görüşü destekleyen yeterli veri bulunmadığını belirterek ilacın piyasadan çekilmesini gerekli bulmadığını açıklamıştır. Takiben pioglitazonun kardiyovasküler olay ve mortalitesi üzerine etkisini araştıran PROactive çalışması ile pioglitazonun infarktüs, inme ve kardiyovasküler olaylar üzerinde olumlu etkileri olduğu açıklanınca, her iki tiazolidinedion arasında kardiyovasküler riskin farklı olduğu yönündeki tartışmalar başlatılmıştır. Rosiglitazonun kardiyovasküler etkilerine yönelik tartışmalara açıklık getiren Haziran 2009 tarihinde açıklanan RECORD (Rosiglitazone Evaluated for cardiovascular Outcome and Regulation of Glycaemia in Diabetes) ve BARI-2 çalışmalarıdır. Her iki çalışmada rosiglitazonun ne pioglitazondan ne de diğer oral antidiyabetik ilaçlardan farklı olmadığı yönünde kanıtlar ortaya konmuştur. Buna rağmen kardiyovasküler olay riskini artırabileceği gerekçesiyle rosiglitazon etken maddeli ilaçlar Avrupa ülkelerinde ve ülkemizde Eylül 2010 tarihinde kullanımdan kaldırılmıştır. ABD ve diğer bazı ülkelerde seçilmiş olgularda kullanımına devam edilmektedir.
Bu makalede ülkemizde var olan pioglitazonun özellikleri anlatılacaktır.
Etki mekanizması: Şekil 7’de gösterilmiştir. Peroksizom Proliferatör-Aktivatör Reseptör-g (PPAR-g) aslında iskelet ve kas hücrelerinde mevcut olan, ancak ön planda yağ dokusunda bulunan bir nükleer reseptörüdür. Tiazolidinedionlar PPAR-g için farmakolojik ligand görevi görür. PPAR-g’nın aktivasyonu DNA’da spesifik elementlere bağlanmayı sağlar, karbonhidrat ve lipid metabolizmasında görevli çeşitli genlerin transkripsiyonunu değiştirir. Bu etkilerden bir tanesi hücre membranında glukoz taşıyıcılarının ekspresyonudur; GLUT-1 ve GLUT-4’ün de ekspresyonunu ve hücre zarına translokasyonunu artırır ve hızlandırır. Böylece karaciğer ve iskelet kasında glukoz uptake artar, kan şekeri düşer.
Glukoz kullanımının büyük bir kısmı kaslarda gerçekleşse de PPAR-g ekspresyonu yüksek oranda yağ dokusunda görülür, yağ dokusundaki PPAR-g aktivasyonu sonucu adiposit diferansiyasyonu sağlanır ve serbest yağ asitlerinin alınması ve depolanması gerçekleştirilir. Depolanma, viseralden ziyade subkütan adipoz dokudadır. Sonuçta dolaşımdaki serbest yağ asitleri azalır, böylelikle insülin direnci de azalmış olur. Öte yandan PPAR-g’nın aktivasyonu yağ dokusu kaynaklı inflamatuvar sitokinleri (TNF-α’yı) azaltır; adinopektin üretimini artırır. Yağ ve kas dokuları arasındaki ara sinyaller; serbest yağ asitleri, leptin, resistin, adiponektin ve doku nekrozu faktörü-a gibi transkripsiyon faktörleriyle gerçekleştirilir.
Tiazolidinedionlar insülin duyarlılığını artırmaları nedeniyle pankreas beta-hücrelerinden insülin sekresyonunun daha az miktarlarda salınımına olanak sağlar. Böylelikle bu ajanlar beta-hücrelerinin yaşam süresini artırır. Beta-hücre fonksiyonlarını koruyucu yöndeki bu etkileri yapılan deneysel ve klinik çalışmalarla gösterilmiştir.
Etkinliği: Pioglitazon oral alındıktan sonra hızla emilir, büyük oranda karaciğerde CYP450 izoenzimler ile metabolize edilir. Çoğu dışkı, az bir kısmı idrarla atılır. Yarılanma ömrü aktif metabolitleri nedeniyle uzun (16-24 saat) etki süresine sahiptir. Günlük dozu 15-45 mg’dır.
A1c’yi düşürme oranları sülfonilüre ve metformine benzerdir, fakat etkinin başlangıcı, gen ekspresyonunu gerektirdiğinden, etkinlik rölatif olarak daha geç başlar. Mikro ve makrovasküler son noktalar üzerine olan etkileri konusunda uzun vadeli veri henüz yoktur. Monoterapide tıbbi beslenme tedavisi ile beraber, kombine tedavide metformin ya da sülfonilürelere ek olarak kullanılabilir. Kalp yetmezliği riskindeki artış nedeniyle insülinle birlikte kullanımı önerilmemektedir.
Glisemik kontrol sağlamalarının ötesinde birçok yararlı kardiyovasküler etkileri olduğuna dair güçlü kanıtlar vardır. Bu yararlar arasında kan basıncını ve trigliseridleri düşürmesi, HDL-kolesterol düzeyini yükseltmesi ve subklinik vasküler inflamasyonu azaltması sayılabilir. Ayrıca, pek çok klinik ve deneysel çalışmada idrar albumin atılımını azalttığı gösterilmiştir. Metabolik sendrom bileşenlerinden olan hiperlipidemi üzerinde pioglitazonun etkileri olumludur; LDL-kolesterol düzeylerini artırmazken; trigliserid düzeyinde azalma yönünde etkili olduğu gösterilmiştir. Ayrıca, PAI-1 düzeyini azaltıp, yağ asitlerini de %20-25 düşürerek insülin direncini azaltmakta; bu nedenle de endotel fonksiyonlarını iyileştirmektedir.
Yan etkileri: Tiazolidinedionların en önemli yan etkileri kilo artışı ve konjestif kalp yetmezliğidir. Tiazolidinedionlar ile görülen kilo artışı doza ve kullanım süresine bağlı olarak görülmektedir. Kilo artışı özellikle periferik subkütan yağ dokusundaki artışa (yeni adiposit oluşumuna) ve periferik ödeme bağlıdır; özellikle insülinle birlikte yüksek konsantrasyonlarda tiazolidinedion kullanıldığında ödem oranı %15’lere çıkabilir. Ödemin muhtemel sebebi böbrek toplayıcı kanallarında var olan PPAR-g reseptörleri üzerinden sodyum reabsorpsiyonunun artışıdır. Ödemin önemli bir özelliği, tedavide diüretik ve anjiyotensin dönüştürücü enzim inhibitörlerine yanıtın yetersiz kalması ve ilacın kesilmesiyle tablonun düzelmesidir.
Bu önemli yan etkilerinden dolayı 2003 yılında ADA ve AHA (Amerikan Kalp Birliği) tiazolidinedion kullanımı ile ilgili bir rapor hazırlamıştır. 2007 yılında revize edilen bu rapora göre tiazolidinedionlar, New York Kalp Cemiyeti kriterlerine göre (NYHA) sınıf I-IV olan tüm hastalarda kontrendikedir. Kullanımı sırasında kilo artışı ve ödem gelişirse hastalar kalp yetmezliği açısından dikkatli bir şekilde değerlendirilmelidir.
Grubun ilk üyesi troglitazonun ciddi hepatotoksisitesi ve ölüm raporları nedeniyle piyasadan çekilmesine rağmen, pioglitazon için bu konuda önemli bir veri bildirilmemiş; aksine karaciğer enzimlerini düşürdüğü gösterilmiştir. Yine de karaciğer yetmezliği olan, karaciğer enzimlerinin normal değerin 2.5-3 katı yüksek bulunduğu hallerde tiazolidinedion kullanılmamalıdır. Diğer yan etkiler anemi ve baş ağrısıdır. Ciddi hipoglisemi yapmaz, ancak hipoglisemiye yol açan diğer oral antidiyabetik ilaçlarla kullanıldığında dikkatle kullanılmalı ve hasta yakından izlenmelidir.
Tiazolidinedionlarla ilişkili bir diğer tartışmalı konu kırık riskini artırıcı etkileri olup olmadığıdır. Pioglitazonun postmenopozal kadınlarda ve ileri yaştaki erkeklerde kırık riskinde artışa yol açtığı bildirilmiştir.
Son yıllarda ileri sürülen bir başka yan etki de makula ödemi sıklığını artırdığı yönündeki bilgilerdir. Özellikle ödem saptananlarda riskin arttığı; bu nedenle ödem gelişmiş olan hastaların makula ödemi açısından da değerlendirilmesi önerilmektedir.
Yakın zamanda sonuçları açıklanan iki gözlemsel (Fransız Ulusal ve USA Kaiser Permanente Sağlık Sigortası verileri) çalışma, pioglitazonu özellikle uzun süre ve yüksek doz kullanan erkeklerde mesane kanseri riskinde artış olduğunu ortaya koymuştur. Bu gelişme üzerine Fransa ve Almanya’da bu ilacın yeni olgularda kullanılması durdurulmuştur. Pek çok araştırıcı, konunun kesinliğe kavuşturulması için ileriye dönük, uzun süreli izlem çalışmalarına ihtiyaç olduğunu vurgulamakta ve bu risk artışına rağmen, diğer antidiyabetik tedavilerin yeterli olmadığını, pioglitazon tedavisinden yarar görebilecek hastalar olduğunu belirtmektedir. Ancak bu grup hastalarda da mesane kanseri ve ilaca bağlı diğer riskleri en aza indirmek için bazı tedbirlerin alınması önerilmiştir. Bu öneri doğrultusunda ileri sürülen görüşe göre:
• Aktif veya mesane kanseri öyküsü bulunan veya sebebi belli olmayan makroskobik hematürisi olan diyabetlilerde pioglitazon kullanılmamalıdır.
• Halen pioglitazon kullanmakta olan ve hematüri, dizüri, pollaküri, bel ve karın ağrısı gibi yakınmaları olan hastalarda mesane kanseri yönünden gerekli tetkikler yapılmalıdır.
• Pioglitazon başlanması düşünülen hastalarda mesane kanseri risk faktörleri (yaş, sigara vs.) sorgulanmalı, fizik muayene ve tam idrar analizi yapılmalı, yarar gözetilenlere ilaç başlanmalıdır.
• Özellikle yaşlılarda pioglitazon verilmesi gerekiyorsa, mümkün olan en düşük dozda başlanmalı, uzun süreli kullanımdan kaçınmalıdır.
Kontrendikasyonları: Pioglitazon, konjestif kalp yetmezliğinin tüm evrelerinde, insülin kullanan hastalarda, Tip 1 diyabetlilerde, kronik böbrek yetmezliği olanlarda, çocuk yaş grubu ve puberte dönemindeki bireylerde, gebelikte, aktif karaciğer hastalığı (SGPT düzeyinin > 3 katı yüksek olduğu durumlar) ve osteoporozisi olanlarda, mesane kanseri riski yüksek olanlarda kontrendikedir.
Özetle; tiazolidinedionlar antihiperglisemik etkinliklerinin yanı sıra hiperinsülinemiyi azaltarak, endotel fonksiyonunu iyileştirerek, mikroalbuminüri ve inflamatuvar belirteçleri azaltarak, dislipidemi (özellikle HDL-kolesterol düzeyinde) ve daha az olarak da kan basıncında iyileşmeler yaparak kardiyovasküler hastalık gelişimini engelleyen ilaçlardır. Özellikle konjestif kalp yetmezliği ve kilo aldırıcı yan etkileri nedeniyle günümüzde tedavinin birinci basamağında tercih edilen ajanlar değildir. İnsülin direnci ön planda olan hastalarda metformine eklenecek bir oral antidiyabetik ilaç düşünüldüğünde iyi bir seçenektir. En önemli yan etkileri kilo artışı, konjestif kalp yetmezliği, anemi, postmenopozal kadın ve erkekte kemik fraktürlerine yol açmasıdır. Konjestif kalp yetmezliğinin tüm evrelerinde, Tip 1 diyabetlilerde, kronik böbrek yetmezliği olanlarda, çocuk yaş grubu ve puberte dönemindeki bireylerde, gebelikte, aktif karaciğer hastalığı ve osteoporozisi olanlarda, mesane kanseri riski yüksek olanlarda kontrendikedir.
C. İNSÜLİN SALGILATICI (SEKRETOGOG) İLAÇLAR
Bu grupta pankreas beta-hücrelerinden insülin salınımını artıran sülfonilüreler ile etki mekanizması benzer, ancak etki süresi daha kısa olan glinidler (meglitinid analogları) yer alır (Tablo 12).
Sülfonilüreler
1942 yılında tifo tedavisinde kullanılan gliprotiyazol isimli ilacın hipoglisemik etkisinin tesadüfen fark edilmesiyle geliştirilen ilaçlardır. Gliprotiyazolün etkisinin daha da geliştirilmesi ve toksik etkisinin azaltılmasıyla önce birinci kuşak sülfonilüreler olarak adlandırılan tolbutamid, klorpropamid, tolazamid ve asetohekzamid elde edilmiştir. Sonraki yıllarda yan etkileri nedeniyle klinik kullanımları sınırlanmış; moleküler yapılarında değişiklikler yapılarak etkileri daha güçlü olan ikinci kuşak sülfonilüreler geliştirilmiştir. İkinci kuşak ajanlar günümüzde beslenme düzeni ve egzersize yanıtsız Tip 2 diyabetlilerde vazgeçilmez ilaçlardandır.
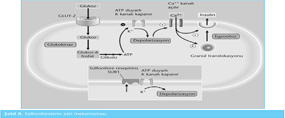
Etki mekanizmaları: Sülfonilüre bileşikleri etkilerini pankreas üzerinde gösterir. Sülfonilüreler beta-hücreleri üzerindeki sülfonilüre reseptörlerine (SUR) bağlanınca ATP’ye duyarlı potasyum (KATP) kanalları kapanır. KATP kanalları iki tip alt üniteden oluşur. Kir 6.2 ünitesi yönlendirme işlemi yaparken, SUR-1 subünitesi kanalın açılıp kapanmasını düzenler. SUR’ların farklı organlarda; örneğin adipoz dokuda SUR2B/Kir6.1, kardiyak miyozitlerde ve iskelet kasında SUR2A, düz kaslarda SUR2B gibi çeşitli izoformları da vardır. Sekretogogların hepsi SUR-1 alt ünitesine bağlanarak etki gösterir. Bağlanma afinite ve kinetiklerine göre sülfonilürelerin farmakolojik özellikleri şekillenir. Sekretogogun SUR’a bağlanmasıyla beta-hücresi membranı depolarize olur, kalsiyum (Ca) kanalları açılarak intraselüler alana kalsiyum geçer ve sonuçta kazanılan enerji ile beta-hücresinde sentezlenmiş insülin içeren, sekresyona hazır granüllerin hücre yüzeyine ulaşması ve granüllerde depolanmış insülinin pinositozla sekrete edilerek portal dolaşıma geçmesi sağlanır. Sonuç olarak sülfonilüre preparatları insülin biyosentezini değil, insülin sekresyonunu primer yoldan, yani glukozdan bağımsız olarak uyarır; suboptimal glukoz konsantrasyonunda da devam edebilir (Şekil 8).
Bundan dolayı sülfonilüreler normogliseminin üzerindeki herhangi bir glisemi düzeyinde daha fazla insülin salınımı sağlar, bu da Tip 2 diyabetin karakteristiği olan insülin sekresyon defektini kısmen düzelterek dolaşımdaki insülin konsantrasyonlarını belirgin olarak artırır, böylelikle insülin direncini kısmen düzeltmiş olur.
Sülfonilürelerin birincil etki mekanizması pankreatik beta-hücrelerinden insülin salınımını sağlamak ise de yapılan çalışmalarda ekstrapankreatik etkileri olduğu da gösterilmiştir.
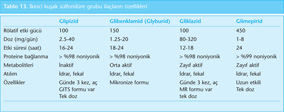
İkinci kuşak sülfonilüreler: Birinci kuşak ilaçlardan 100-200 kat daha potent ilaçlardır. İlaçların bazı özellikleri Tablo 13’te gösterilmiştir. Absorpsiyon, metabolizma ve eliminasyon yönünden farklılıklar gösterir. Genellikle karaciğerde metabolize edilir, idrar ya da safra yoluyla atılır. Birinci kuşak sülfonilürelerin aksine plazma proteinlerine iyonik bağlanmazlar, bu nedenle ilaç etkileşimleri daha düşüktür. APG düzeyinde ortalama 60-80 mg’lık bir düşüş sağlayabilirler; plaseboya göre A1C düzeyini ortalama %1-2 düşürür. Bugün kullanımda olanlar arasında küçük farklılıklar olmasına rağmen etkinlikleri eşittir. Etkinliği belirleyen preparatların absorpsiyonlarının farklı olmaları ve hastaların kişisel farklılıklarıdır. Yemekten 30 dakika önce verilmelidir. Düşük dozdan başlayarak istenilen kontrol sağlanana kadar 4-7 gün aralıklarla doz artırılır. Genel olarak önerilen maksimum dozun yarısına gelindiğinde sülfonilürelerin glukoz düşürücü etkisi plato yapar. Bu nedenle submaksimal doza ulaşıldığı halde yeterli etkinlik sağlanamayan durumlarda; sülfonilüre dozunu artırmak yerine; farklı etki mekanizmalı başka bir oral hipoglisemik ajan ile kombine edilmesi önerilmektedir. Sülfonilüreler monoterapide ve insülin dahil diğer tüm antihiperglisemik ajanlarla kombine kullanım için onaylanmıştır.
Sülfonilürelere yanıtsızlık: Sülfonilüre başlandıktan sonraki ilk ay içinde hastaların %5-10’unda yanıt alınamaz. Buna “primer yanıtsızlık” adı verilir. Bazı hastalarda ise sülfonilürelerle sağlanan iyi glisemik kontrol yıllar içerisinde bozulabilir. On yıl sülfonilüre kullananların %50-75’inde sülfonilürelere yanıtsızlık gelişir. “Sekonder yanıtsızlık” denilen bu tablonun sebepleri hasta, hastalık ya da tedavi ile ilişkili olabilir. Yanıtsızlığı, genellikle ilerleyici beta-hücre yetersizliğine bağlamak mümkündür; yine de sekonder sülfonilürelerle yanıtsızlığında hastanın beslenme düzeni ve egzersiz programına uyumsuzluk olup olmadığı gözden geçirilmeli, dozu artırmak ya da farklı bir sülfonilüre preparatına geçmek yerine farklı fizyopatolojik temelli bir ilaç ya da insüline geçilmesi önerilmektedir.
Yan etkileri: Klinikte en sık ve en önemli yan etkileri hipoglisemi, kilo artışı ve hepatotoksisitedir. Başlıca yan etkiler Tablo 14’te verilmiştir. Hipoglisemi sıklığı ile değişik bilgiler olmasına karşın, sülfonilüre kullanan her beş hastadan birinin altı ayda bir en az bir kez semptomatik hipoglisemiye girdiği bildirilmektedir. Sülfonilürelerin etki süreleri değişken faktörlere bağlı olduğundan bu ajanlara bağlı hipoglisemi geçirenler birkaç gün hastanede izlenmeye alınmalıdır. Kilo artışı açısından bakıldığında; UKPDS çalışmasında da belirtildiği gibi sülfonilüre kullananlarda, metformin kullananlara göre daha belirgin bir kilo artışı olmaktadır. Tablo 14’te gösterilen yan etkilerden hipersensitivite reaksiyonları, flushing, dilüsyonel hiponatremi, guvatr gelişimi birinci kuşak sülfonilüreler ile oluşur; ikinci kuşak sülfonilüre ilaçlarda pek görülmez. Flushing, alkol alımından sonra gelişir. Dilüsyonel hiponatreminin sebebi, sülfonilürelerin renal tubulide ADH’ye duyarlılığı artırmasıdır. Guvatr gelişmesi de iyodun hücre içine girişini engellemesine bağlıdır.
İnsülin direnci ve bunun karşılığı olan hiperinsülinemi dikkate alındığında, yarattığı hiperinsülinemi durumu nedeniyle sülfonilüreler, kullanılmaya başlandığı ilk yıllarda, kardiyak olayları artırabileceğine dair kuşkular uyandırmıştır. Nitekim yeni başlangıçlı diyabet hastalarında insülin tedavisine kıyasla sülfonilüre grubunda mortalitenin daha yüksek olduğu, “University Group Diabetes Program (UGDP) Study” araştırıcıları tarafından bildirilmiştir. Bu bulgular bütün sülfonilüre prospektüslerinde, kardiyovasküler mortalitenin artabileceği uyarısının yazılmasına neden olmuştur. Sülfonilüreler aynı zamanda kalpte bulunan SUR2A reseptörlerine bağlandığında kardiyak KATP kanallarını da kapattığından, iskemiye alışma (ischemic preconditioning) sürecini de bozabilir. Böylece teorik olarak bu self-protektif mekanizmanın aksi yönde etkiye sahip her türlü olay gibi sülfonilüreler de miyokardiyal iskemiyi ve sonuçta miyokardiyal hasarı artırabilir. Ancak sülfonilürelerin kardiyak SUR’a olan afinitesi beta-hücrelerine göre daha düşüktür. Yeni kuşak sülfonilüre gruplarının (özellikle gliklazid, glimepirid) ise yalnızca beta-hücrelerindeki SUR’lara afinitesi olduğu bilinmektedir. Bu nedenle sülfonilürelerin gerçekten kardiyak iskemiye yatkınlık yarattığı ispatlanmamıştır.
Kontrendikasyonları: Sülfonilüre preparatları, hepatik veya böbrek fonksiyonu ileri derecede bozuk olanlarda kullanılmamalıdır. Kontrendike olduğu haller Tip 1 diyabet, sekonder diyabet, akut hiperglisemik komalar, gebelik, ağır infeksiyonlar, travma, majör cerrahi uygulamaları, hipoglisemiye yatkınlık durumları, karaciğer ve böbrek yetmezliğidir.
Özetle sülfonilüreler, insülin sekresyonunu artırarak etkili olan, A1C değerini ortalama %1.5-2 düzeyinde iyileştiren, plazma lipidlerine direkt etkisi olmayan, en önemli yan etkileri hipoglisemi ve kilo artışı olan ve diğer oral antidiyabetik ilaçlara göre pahalı olmayan ilaçlardır.
Glinidler (Meglitinid analogları)
Meglitinid analogları, sülfonilüre yapısında olmayan fakat insülin sekresyonunu stimüle eden yeni, kısa etkili glukoz düşürücü ilaçlardır. Bu grupta bir benzoik asit derivesi olan repaglinid ile fenilalanin derivesi olan nateglinid bulunmaktadır.
Etki mekanizmaları: Beta-hücrelerindeki SUR’a bağlandıklarından etki mekanizmaları sülfonilürelere benzer. Esas farkları, etkilerinin hızlı başlaması ve etki sürelerinin daha kısa oluşudur. Bu etki, doğal olarak yemekle-uyarılan insülin salınımına daha benzer olduğundan bu ilaçlar postprandiyal hiperglisemide daha etkili kontrol sağlar ve daha nadir hipoglisemiye neden olur.
Etkinlikleri: Sülfonilürelere benzer, ancak nateglinidin sekretogog etkisi hafifçe daha düşüktür. Yarılanma ömrü repaglinidin 4-6 saat, nateglinidin 1.4 saat kadardır. Repaglinidin başlangıç dozu her öğün öncesi 0.5 mg’dır, maksimum doz her öğün öncesi 4 mg’a kadar çıkarılabilir. Öğünlerden hemen önce (0-20 dakika önce) alınmalıdır. Nateglinid, çok hızlı ve tam olarak ince bağırsaktan absorbe edilir. Genellikle her yemekten 10 dakika önce 120 mg dozunda verilir, maksimum doz 360 mg’dır. Hem repaglinid hem de nateglinid karaciğerde metabolize olur; repaglinid safra yoluyla, nateglinid böbrekler yoluyla atılır. Repaglinidin %90’ının safra yoluyla atılması ve metabolitlerinin hipoglisemik aktiviteli olmaması nedeniyle hafif-orta böbrek yetmezliğinde rölatif olarak güvenli kullanılacağı düşünülmesine karşın, kural olarak renal fonksiyonların azaldığı durumlarda insülinin de klerensi azalacağından tüm sekretogoglar gibi dikkatli kullanılmalıdır. Bu ajanlar rölatif olarak yeni olduklarından mikrovasküler ve makrovasküler komplikasyon risklerine yönelik etkileri henüz bilinmemektedir, ancak sülfonilüre ile benzer yönde etki göstermeleri beklenebilir. Hem repaglinidin hem de nateglinidin PPAR-g reseptörüne bağlanabildikleri gösterilmiştir.
Yan etkileri: Genel olarak diğer sülfonilürelere benzerse de kilo artış oranı daha az, hipoglisemi atakları daha nadirdir. Ancak daha sık kullanım (günde üç kez) gerektirir ve sülfonilürelerden daha pahalı ilaçlardır. Nateglinidin bu yan etkilere ilaveten baş dönmesi, bulantı, ishal gibi yan etkileri de vardır.
Sekretogoglar monoterapide veya metformin, tiazolidinedion ya da inkretin mimetikler ile kombinasyon yapılarak kullanılabilir; ancak iki sekrotogog, sülfonilüre ve meglitinid analogları birlikte kullanılmamalıdır.
D. İNSÜLİNOMİMETİK İLAÇLAR
Tablo 15’te gösterilen bu grup yeni ilaçlardır; kapsamında amilin agonistleri ve inkretin bazlı tedavi için kullandığımız ilaçlar yer alır. Genel olarak endojen insülin sekresyonunu artırarak etkili olmaktadırlar.
Amilin Analogları
Bir beta-hücre hormonu olan amilinin sentetik analoğu olan pramlintid insülin tedavisine destek amacıyla ABD’de kullanılmaktadır. Tokluk glukoz düzeylerine etkilidir, günde üç kez subkütan enjeksiyon gerektirir.
İnkretin Bazlı İlaçlar
Tip 2 diyabette önemli defektlerden birisi de inkretin hormonların (GLP-1 ve GIP) düzeyi ve/veya etkisinin azalması ve glukagon sekresyonunun inhibe edilememesidir. Bu grupta yer alan ilaçlar inkretin hormonları taklit etmek (GLP-1 agonistleri = inkretinmimetik) ya da inkretinlerin degredasyonunu inhibe etmek (DPP-4 inhibitörleri = inkretin artırıcı) üzere geliştirilmiştir, her iki grubun farkları Tablo 16’da belirtilmiştir.
İnkretinmimetikler (GLP-1 agonistleri): Endojen inkretin olan GLP-1’i taklit ederler. Örnek: GLP-1 reseptör (GLP-1R) agonistleri (Eksendin-4: Eksenatid, eksenatid LAR, liraglutid), subkütan enjekte edilir.
• Eksenatid: ABD’de 2005 yılından beri, Avrupa Birliği ülkelerinde ise 2006 yılından beri kullanılmaktadır. Tip 2 diyabetli hastalarda kullanılan eksenatid, ülkemizde Byetta ismiyle piyasadadır. Günde iki kez enjeksiyon gerektiren ve tokluk glisemisini düşürmede daha etkili olan bu ilaç, diğer antihiperglisemik ilaçlar ve insülinin aksine, ortalama 2-4 kg kilo kaybı sağlamaktadır.
Endikasyonları: Özellikle BKİ ≥ 35 kg/m2 olan kişilerde metformin, sülfonilüre veya tiazolidinedion grubu ilaçlarla kombine olarak kullanılması önerilmektedir. Ancak emniyet açısından 18 yaş altındaki obez Tip 2 diyabetlilerde kullanılmamalıdır. Eksenatid kullanan hastalarda bir yıllık tedavi ile A1C’de %1 azalma olmamışsa ve altı aylık tedavi ile vücut ağırlığında en az %3 azalma sağlanamamışsa tedaviye devam edilmemelidir.
Yan etkisi: Bu grup ilaçlarda en önemli yan etki bulantıdır. Eksenatid piyasaya verildikten sonra akut pankreatit riskinde artış bildirilmişse de diyabetin kendisinin de pankreatit riskini artırması nedeniyle bu konu kesinlik kazanmamıştır. Ancak FDA’nın isteğiyle 2008 yılında ilaç prospektüsüne bu konuda bir uyarı konulmuş ve hekimin eksenatid kullanan hastalarında akut pankreatit kuşkusu (şiddetli karın ağrısı, bulantı-kusma, amilaz/lipaz yükselmesi ve radyolojik bulgular) varsa ilacı hemen kesmesi önerilmiştir.
• Liraglutid: Yurt dışında henüz kullanıma sunulmuş olan bu ilaç eksenatide benzer şekilde etkilidir, günde bir kez enjeksiyon gerektirmektedir. Kullanım endikasyonları ve yan etkileri eksenatid gibidir. Liraglutid kullanımında da pankreatit olguları bildirilmiştir; deneysel çalışmalara dayanarak tiroid bezinde C hücreli hiperplaziyi artırdığı yönündeki kuşkular nedeniyle hastada tedavi öncesi kalsitonin düzeyi bakılması; normal olanlarda takiple başlanması önerilmektedir.
Benzer etkili olan ve FDA’dan henüz kullanım onayı alan Eksenatid LAR ise haftada bir enjeksiyon şeklinde kullanılmak üzere tasarlanmıştır.
İnkretin artırıcı ajanlar (DPP-4 inhibitörleri): Endojen inkretinler GLP-1 ve GIP’ın yıkımını sağlayan DPP-4’ü inhibe eder (sitagliptin, vildagliptin, saksagliptin), oral olarak verilmek üzere geliştirilmiştir. Bu grup ilaçlar genellikle günde bir (gerekirse iki) kez kullanılır, kilo açısından (metformin ve akarboz gibi) nötr etkilidir. Sitagliptin, ülkemizde 2008 yılında Januvia, vildagliptin 2010 yılında Galvus, saksagliptin ise 2011 yılında Onglyza adıyla kullanıma sunulmuştur.
Endikasyonları: Glukoz-bağımlı etki gösterdikleri için hipoglisemiye sebep olmazlar. DPP-4 inhibitörleri sülfonilüre, metformin veya tiazolidinedion grubu ilaçlarla birlikte kullanılabilir. Bu durumda hipo riski olabilir; ilaç dozu düşürülmelidir. Sitagliptinin insülin ile birlikte kullanılmasına FDA onay vermiştir. Ülkemizde metformin ve sülfonilürelerle yeterli kontrol sağlanamamış diyabetlilerde ikinci veya üçüncü seçenek olarak kullanılmasına izin verilmektedir, saksagliptin hariç diğerleri geri ödeme kapsamındadır.
Yan etkileri: Klinik çalışmalarda bu grup ilaçların önemli bir yan etkisi bildirilmemiştir. Ancak pazara sunulduktan sonra bazı hastalarda gribal infeksiyona benzer bir klinik tabloya yol açtıkları görülmüştür. Ayrıca Eylül 2009 tarihinde akut pankreatit olgularının bildirilmesi nedeniyle FDA tarafından ilaç prospektüsüne uyarı konulması istenmiştir. Bununla beraber, konuyu destekleyen klinik kanıtlar bulunmamaktadır. Aynı şekilde yakın zamanda eksenatid ve sitagliptin kullanımında pankreas kanseri riskinin arttığı yönündeki kuşkuları da destekleyen kesin veriler mevcut değildir.
Sonuç olarak GLP-1 analogları ve DPP-4 inhibitörleri monoterapi ya da kombine tedavide kullanılabilen inkretin bazlı tedavilerdir. A1C düzeyindeki iyileşmeler başlangıç düzeyine bağlı olarak monoterapide %0.6-1.1 arasında; kombinasyon tedavisinde 0.7-1.9 arasında değişmektedir. Kilo alımını artırmaz. Hipoglisemi yan etkileri nispeten azdır. Tolerabiliteleri iyidir, pankreas alfa ve beta-hücresi cevaplılığını artırarak adacık fonksiyonlarını düzelttiği gösterilmiştir. Bununla birlikte adacık hücreleri üzerindeki etkileri, uzun dönem mortalite ve komplikasyonlar üzerindeki sonuçları açısından uzun süreli çalışmalara ihtiyaç vardır.
İNSÜLİN
İnsülin Biyosentezi
İnsülin, 11. kromozomdan gelen komutla, pankreas adacık beta-hücrelerinde sentez edilen protein yapısında, anabolik bir hormondur. Sentezin ilk aşamasında preproinsülin adı verilen, 86 aminoasidi olan tek zincirli polipeptiddir; bir sonraki aşamada preproinsülinden proteolitik bir süreçle aminoterminal peptid uzaklaştırılarak proinsülin haline dönüşür. Tek zincir yapısında olan proinsülinden 31 aminoasitlik bir internal rezidü fragmanı connecting peptid (C-peptid) ayrılır; geriye kalan çift sarmal spiral biçimine dönüşerek insülin molekülünü oluşturur. İnsülin molekülü, her birinde 21 ve 30 aminoasit barındıran ve birbirlerine disülfid bağları A ve B zincirlerden oluşmuştur. İnsülin ve C-peptid beta-hücresinde sekretuvar granüllerde depolanır; gerektiğinde sekrete edilir.
İnsülin Sekresyonu
İnsülin sekresyonunu aminoasitler, ketonlar, gastrointestinal peptidler ve nörotransmitterler etkilemekle birlikte, pankreas beta-hücrelerinden insülin sekresyonunun anahtar düzenleyicisi glukozdur. Kandaki 70 mg/dL değerinin üzerindeki glukoz düzeyleri, primer olarak protein translasyonunu artırarak ve insülin sekresyonunu da indükleyerek insülin sentezini stimüle eder. İnsülin sekresyon profili ile ilgili çalışmalar hormonun salınımının pulsatil olduğunu göstermektedir. Yaklaşık her 10 dakikada bir küçük sekretuvar pikler, 80-150 dakikalık daha geniş osilasyonlarda süperempoze olmaktadır. Saatte 1-2 U dozunda sürekli salgılanan bu insülin bazal insülindir; başlıca etkisi karaciğerden glukoz çıkışını kontrol etmektir. Öğünler ya da sekresyonu sağlayan diğer stimülanlar, bazalin 4-5 kat fazlası büyüklüğündeki pikleri indükler; sonrasında bazale dönüş genellikle 2-3 saati bulmaktadır. Her yemekle birlikte beta-hücre sekretuvar granüllerinden sekrete edilen insülin, bolus (prandiyal) insülindir. Günlük salınan insülinin %50’si bazal, %50’si bolus formundadır. Fizyolojik konsantrasyonlarda dolaşımdaki insülin monomer yapıdadır.
İnsülin Etkisi
İnsülin, portal sisteme sekrete edildikten sonra, ilk durağı karaciğerde %50 oranında kullanılır. Geri kalanı sistemik dolaşıma geçerek periferik hücrelerdeki hedef reseptörlerine bağlanır. Bu bağlanma intrensek tirozin kinaz aktivitesini stimüle ederek, reseptör otofosforilasyonuna ve insülin reseptör substrat (IRS) gibi hücre içi sinyal moleküllerinin tetiklenmesine yol açar; böylelikle insülinin metabolik ve mitojenik etkileriyle sonuçlanan fosforilizasyon kaskadı başlatılır. Bu olay hücrelere glukoz alınmasını sağlayacaktır. Glukoz homeostazisi; karaciğerden glukoz üretimi ile periferik hücrelerin glukoz alımı ve kullanımı arasındaki ince çizgiyi yansıtır. İnsülin bu dengenin en önemli düzenleyicisidir.
İNSÜLİN PREPARATLARI ve KULLANIM İLKELERİ
Tarihçesi
İnsülinin bilinmediği yıllarda diyabet ölümcül bir hastalıktı. 1921 yılında Kanadalı Cerrah F.G. Banting ve öğrencisi C. Best’in insülini keşfetmesi, Fizyolog J. McLeod ve Biyokimyacı J. Collip’in katkılarıyla geliştirilen ekstrenin Tip 1 diyabetli bir hastaya uygulanmasıyla diyabette yeni bir çığır açılmış; bu buluş kaşiflerine Nobel ödülü kazandırmıştır. 1936 yılında Hagedorn balık protamini eklenmesinin insülini süspansiyon halinde tuttuğunu, böylelikte enjekte edildiği subkütan dokudan emiliminin yavaşladığını gözlemlemiş; sonuçta orta etkili (NPH) insülini keşfetmiştir. Scott ve Fisher de benzer biçimde çinko eklenmesiyle de insülinin etkisinin daha fazla uzatılabileceğini göstermişlerdir. Sonraki yıllarda 1958 yılında F. Sanger’in insülin aminoasit dizilimini göstermesi, 1964 yılında D. Hodgkin’in kristal yapısını ortaya koyması ve R. Yalow’un RIA (Radio Immuno Assay) yöntemlerini geliştirmesi diğer Nobel ödüllü buluşlardır.
İnsülinin Yapısı ve Üretimi
İnsülin birbirine disülfit bağlarıyla bağlanmış, 21 aminoasitli A ve 30 aminoasitli B olmak üzere, iki zincirden ibarettir. İnsülin tarihinin ilk 60 yılında insülin sadece sığır ve domuz preparatları şeklinde kullanılmaktaydı. Yapısı bakımından insan (human) insülini ile kıyaslandığında sığır insülini üç, domuz insülini ise yalnızca bir aminoasit farklıdır. 1980’li yıllarda insan insülini devreye girerek hayvansal kökenli insülini devre dışı bırakmıştır. Günümüzde artık rekombinant DNA teknolojisi ile insan insülinine benzer insülin üretilmektedir; bu amaçla genetik yapısı değiştirilmiş bakteri suşları (Escherichia coli) ve mayalar (Saccharomyces cerevisiae) geliştirilmiştir. Bu tip insülinlerin antijenik özelliği düşük olmakla birlikte yüksek konsantrasyonlarda dimer ve hekzamer oluşturma eğiliminde oldukları görülmüştür. Bu nedenle de enjekte edildiği dokudan dolaşıma absorpsiyonları yavaştır; bu durum kliniğe insülin absorpsiyonu ve glukoz emilimi arasındaki uyumsuzluk olarak yansır. Bu nedenle insülin molekülünde bir ya da daha fazla aminoasitte yapılan yapısal değişikliklerle insülin analogları geliştirilmiş, böylece insülinin fiziksel ve farmakolojik özelliklerinin değiştirilmesi sağlanmış ve insülin tedavisini hastanın yaşam stiline uygun esneklikte uygulamak imkanı doğmuştur. Geçmiş 80 yılda insülinin formül yapısının gelişmesi, evde şeker ölçümleri ile glukoz izleminin kolaylaşması ve fizyolojik insülinemi gereksinimlerinin daha iyi anlaşılmasıyla diyabet tedavisinde büyük adımlar atılmıştır. Ancak fizyolojik insülinemi sağlama amacımıza çok yakın olmakla birlikte, insülini fizyolojik olmayan bir bölgeye, yani subkütan dokuya uyguluyor olmanın doğal sınırlandırmaları nedeniyle bu amaca halen ulaşılamamaktadır.
İnsülin Tipleri
Halen kullanılmakta olan insülin preparatları farmakokinetik özelliklerine göre tanımlanabilir; etki profillerine göre, hızlı-kısa, kısa (regüler = kristalize), orta (NPH) ve uzun etkili olmak üzere gruplandırılır. Ayrıca kısa ve orta etkili insülinleri bir arada bulunduran mikst formlar (karışım human ve karışım analog insülinler) geliştirilmiştir (Tablo 17).
Tablo 17 tedavide kullanılan insülinlerin subkütan enjeksiyonundan sonra etkinin başlama zamanı, maksimum etki zamanı ve etki sürelerini göstermektedir. Bu insülinler ile farklı zaman-etki profilleri ile fizyolojik insülinemiyi taklit etme amacına ulaşmak mümkün olabilmektedir (Şekil 9). İnsülin replasmanı, öğün öncesi (bolus) ve bazal insülinler olarak düşünülmelidir. Bolus insülinler, hızlı etkili analoglar veya kısa etkili regüler insülinlerdir; yemek sonrasında görülen insülin düzeylerine benzer etki sağlamak amacıyla kullanılır. Bazal insülinler orta ve uzun etkili insan insülinleri ve analog insülinleridir; öğünler arasında, gece boyunca ve açlık durumundaki bazal insülinleri taklit etmeyi sağlarlar.
a. Öğün öncesi (bolus) insülinler: Regüler ve analog insülinlerdir.
Kısa etkili insan insülini (human regüler insülinler): Etkisi enjeksiyondan 30-60 dakika sonra başlar, 2-4 saat sonra en yüksek etki düzeyine ulaşır ve etki süresi 5-8 saat sürer. Enjekte edildiği subkütan dokudan emilimi yavaştır; bu nedenle öğün süresi karbonhidrat emiliminin pik süresiyle insülin emiliminin kinetiklerini eşleştirmek için regüler insülin yemekten 30-45 dakika önce uygulanmalıdır.
Hızlı-kısa etkili insülin (prandiyel analog insülin): Regüler insülinin zaman-etki profili fizyolojik insülin salgısını taklit etmede yetersizdir. Çözeltideki hekzamer yapısındaki insülinin subkütan enjeksiyonundan sonra dolaşıma karışabilmesi için monomer yapısına çözülmesi gerekir. Bu nedenle hekzamerlerden monomere hızla dönüşebilen, çözelti içinde daha az kalan; bu nedenle daha hızlı emilerek etkisi hızlı başlayan insülin analogları geliştirilmiştir. Günümüzde piyasada olan üç hızlı-kısa etkili analog (lispro ve aspart glulisin insülinler) vardır.
• Lispro insülin: İnsanlara uygulanması ilk onaylanan insülindir. B zincirindeki prolin ve lizin yer değiştirilmiş; böylelikle bağlanma özelliği azaltılarak enjekte edildiği dokudan emilimi hızlandırılmıştır. Etkisi 15 dakikada başlar, biyolojik etkinlik piki 60-90 dakika, etki süresi 4-5 saattir. Uygulamada yemek öncesinde 30 dakika bekleme zorunluluğu olmaması nedeniyle öğün zamanlarında daha fazla esneklik sağlar; doz öğündeki karbonhidrat içeriğine göre düzenlenebilir. Sürekli cilt altı insülin infüzyon pompa tedavisinde tercih edilen bir insülindir. Etkisinin hızlı oluşu ve erken postprandiyal hipoglisemi olasılığı nedeniyle gastroparezili hastalarda dikkatli kullanılmalıdır. Gastroparezisi olanlarda hipoglisemi riskini azaltmak için insülin enjeksiyonu yemeğini bitirdikten sonrasına ertelenebilir. Noktürnal hipoglisemi riski düşüktür.
• Aspart insülin: Lisproya benzer şekilde subkütan enjeksiyondan sonra hızla emilir, regüler insülin ile elde edilenden daha yüksek pik konsantrasyona yükselir. Hem Tip 1 diyabetli, hem de Tip 2 diyabetli hastalarda regüler insülinle kıyaslama yapılan çalışmalarda hipoglisemi riskinde fark olmaksızın A1C düzeylerinde anlamlı azalma olduğu saptanmıştır. Sürekli cilt altı insülin infüzyon pompa tedavisinde de etkinlik ve güvenilirliği gösterilmiştir.
• Glulisin insülin: İnsülin aminoasit diziliminde yapılan değişikliklerle etkinliği hızlandırılmış bir başka analog insülindir. Ülkemizde mevcuttur.
b. Bazal insülinler: Salgılanan günlük insülin dozunun %50’si bazal insülin olup, yemek aralarında ve açlık döneminde normogliseminin sürdürülmesini sağlar. Bu nedenle tedavide de fizyolojik insülinemiyi taklit etmek üzere etkisi uzatılmış insülinler geliştirilmiştir. Bu grupta orta etkili (human NPH ve lente) ve uzun etkili (ultralente) insan insülinlerini ve uzun etkili insan analog insülinlerini (bazal analog) sayabiliriz.
Orta etkili insülinler: Enjekte edildiği subkütan dokudan emilimini geciktirmek, böylelikle etkisini uzatmak için geliştirilen süspansiyon formlarıdır. NPH insülinin etkisi, 1.5-3 saatte başlar, maksimum etkiye 5-7 saatte ulaşır; etkisi 12-16 saat sürer. Lente insülin çinko ile süspansiyon haline getirilmiş, benzer etkiye sahiptir. Ülkemizde kullanılmamaktadır. Orta etkili insülinler uzatılmış etkileri nedeniyle öğün sonrası serum glukoz düzeylerini kontrol etmede uygun değildir. Bu nedenle sabah-akşam veya sabah-gece olacak şekilde günde iki doz olarak kullanılır. Günümüzde kalem formu geliştirilmiş tek orta etkili insülin human NPH insülindir.
Uzun etkili insan insülini: Ultralente insülindir. Enjeksiyondan dört saat sonra başlayan, maksimum etkiye 8-10 saatte ulaşan ve etki süresi 20 saat süren insülindir. Ülkemizde kullanılmamaktadır.
Uzun etkili analog insülinler (Bazal analog da denir): Klinik kullanımda glarjin ve detemir insülin olarak bilinen olan iki formu vardır.
• Glarjin insülin: İnsülin molekül yapısında yapılan aminoasit değişiklikleriyle moleküle yüksek izoelektrik noktada olabilme özelliği sağlanmış; böylece enjekte edildiği noktada dokunun nötral ortamında çökerek etki süresinin uzatılması mümkün hale getirilmiştir. Belirgin pik etkisi olmaksızın 24 saat etki süresine sahiptir. Noktürnal hipoglisemi riskini azaltır. İnsülin benzeri büyüme faktörü 1 (IGF-1) reseptörlerine insan insülininden daha fazla afinite gösterir. Bu afinitenin IGF-1 reseptörlerinden zengin hücre dizilerinde mitojenik etki potansiyelinin artışına neden olabileceği düşünülmektedir. Bu düşüncenin klinik anlamı henüz bilinmemektedir.
• Detemir insülin: Albumine bağlanma ile geliştirilmiş olan bir başka uzun etkili analog insülindir. B zinciri 30. pozisyondaki aminoasit kaldırılarak 29. pozisyondaki aminoaside alifatik yağ asidi açillenmiştir. Bu değişiklik albumin ve açillenmiş yağ asidi arasında geri dönüşlü bağlanmayla sonuçlanır. Enjeksiyondan sonra insülinin %98’i albumine bağlanır; bağlanma bölgesinden yavaş olarak ayrılması etkisinin uzamasını sağlar. Zaman-etki profili 6-8 saat maksimum etki ve 24 saate varan etki süresidir.
c. Karışım human ve analog insülinler: Kısa ve orta etkili insülinlerin değişik oranlarda karışım preparatları geliştirilmiştir. Bu insülinlerin kullanılması, hastanın kendi yaptığı karışımın olası sorunlarını önler, enjeksiyon öncesinde yapabileceği hataları minimale indirir. Buna karşın öğün öncesinde ve bazal insülin dozlarında kolay düzenleme yapılmasına fırsat vermez. Bu nedenle standart öğün tüketimi olan Tip 2 diyabetlilerin tedavisinde yeri olan insülinlerdir. Yaşlı hastalarda, görme ya da motor hareket bozukluğu olanlarda enjeksiyon sayısını azaltması nedeniyle tercih edilir. Karışım analogların, human karışım preparatlarına oranla daha iyi postprandiyal glukoz düzeyi ve daha az hipogoglisemi sağladığı gösterilmiştir.
İnsülin Enjeksiyonu Ne Zaman Yapılmalıdır?
Uygulama insülin tipine göre değişir.
• Hızlı etkili insülinler yemekten 5-15 dakika önce, kısa etkililer ise yemekten 30 dakika önce uygulanmalıdır.
• Kan glukoz düzeylerine göre de insülin enjeksiyon zamanı değiştirilebilir. Örneğin; öğün öncesi plazma glukoz hedeflenen değerden yüksek ise yemek zamanı biraz geciktirilebilir.
• Mide boşalma zamanı aşırı uzamış diyabetli bireylerde, hipoglisemilerden korunmak için insülin enjeksiyonu yemekten sonraya geciktirilebilir.
İnsülin Preparatları Karıştırılarak Kullanılabilir mi?
• Kısa etkili ve NPH insülinler aynı enjektöre çekilerek uygulanabilir; insülinler karıştırıldıktan sonra bekletilmeden, hemen kullanılmalıdır (bazı kaynaklar ise bu karışımların buzdolabında iki haftaya kadar muhafaza edilebileceklerini bildirmektedir).
• Glargin ve detemir insülinler diğer insülinlerle karıştırılmamalıdır.
İnsülinin Saklanma Koşulları
Protein yapısında, oral kullanımı olmayan insülin preparatlarının flakon (vial) ya da kartuş olarak geliştirildiğini belirtmiştik. Açılmamış insülin flakon ve kartuşları son kullanım tarihine kadar buzdolabında 2-8°C’de saklanabilir. Açılmış kartuş ve flakonlar, aşırı sıcak olmamak koşuluyla oda ısısında 30 güne kadar kullanılabilir. Orta/uzun etkili veya karışım insülin preparatları açıldıktan 15 gün sonra biyolojik aktivitelerini hafifçe yitirmeye başlar. Hasta ve hastalıktan kaynaklanan şartlar değişmediği halde glisemik kontrol bozulmaya başlarsa bu faktör göz önünde bulundurulmalıdır.
İnsülin Tedavisinde Amaç
Hiperglisemi semptomlarını düzeltmek, akut komplikasyonları önlemek, mikro ve makrovasküler komplikasyonları önlemek ve geciktirmektir. Tip 1 diyabetli hastalarda hem bazal insülin sekresyonu hem de yemek sonrası insülin pikleri kaybolmuştur. Bu nedenle tedavide en mantıklı yaklaşım bazal-bolus insülin sekresyonlarını sık aralıklı insülin enjeksiyonlarıyla yerine koyarak fizyolojik insülinemiyi taklit etmektir (Şekil 9); Tip 2 diyabette ise bazı durumlarda (bazal) insülin desteği gereksinimi doğar; hastalık ilerledikçe zaman içinde insülin replasmanına ihtiyaç olabilir.
İnsülin Endikasyonları
İnsülinin eksik ya da etkisiz olduğu aşağıdaki durumlarda insülin kullanılır.
1. Klasik Tip 1 diyabet ve LADA olguları,
2. Hiperglisemik aciller (DKA ve hiperglisemik nonketotik koma),
3. Aşağıda ifade edilen bazı durumlarda Tip 2 diyabet,
• Oral antidiyabetik ilaç ile iyi metabolik kontrol sağlanamaması durumunda,
• Aşırı kilo kaybı olanlarda,
• Ağır hiperglisemik semptomlar bulunanlarda,
• Akut miyokard infarktüsü geçirmekte olan diyabetlilerde,
• Akut ateşli, sistemik hastalığı olanlarda,
• Hiperozmolar hiperglisemik durum (HHD) veya ketotik koma (DKA) olan durumlarda,
• Majör cerrahi operasyon geçirecek olanlarda,
• Gebelik ve laktasyon döneminde,
• Böbrek veya karaciğer yetmezliği olan diyabetlilerde,
• Oral antidiyabetik ilaçlara allerji veya ağır yan etkiler gelişenlerde,
• Ağır insülin direnci (akantozis nigrikans) bulunan diyabetlilerde,
4. Diyet ile kontrol altına alınamayan gestasyonel diyabet.
İnsülin Uygulaması
Peptid yapısında üretilen bir hormon olduğundan oral kullanımı yoktur. Genelde subkütan uygulanır, kısa ya da hızlı-kısa etkili olanlar intravenöz (IV) ya da intramusküler (IM) yoldan kullanılabilir. 10 mL’lik şişe (vial) ya da 3 mL’lik kartuş olarak üretilmektedir. Tüm dünyada global olarak 1 mL’de 100 IU bulunan “U-100” insülinler kullanılmaktadır (ayrıca, bazı Avrupa ülkeleri ve ABD’de insülin gereksinimi çok yüksek olan insülin dirençli hastalar için U-500 insülinler bulunmaktadır).
Enjeksiyon, aslında vücudun sağlam olan her bölgesinde uygulanır olmakla birlikte genelde, Şekil 10’da gösterilen vücut bölgelerinden rotasyon usulü ile uygulanır. İnsülin kaynağı, enjeksiyon yeri, ortam ısısı enjekte edildiği bölgede insülin absorpsiyonunu hastadan hastaya değiştirebilir: Örneğin; İnsan insülini hayvansal kaynaklı insülinlere göre daha kısa etkilidir. Enjeksiyon yeri göz önüne alındığında en hızlı emilim yeri abdomendir. Daha sonrasında en hızlıdan yavaşa doğru kol, uyluk ve kalçadır. Sıcakta insülin absorpsiyonu daha çabuk, soğukta daha yavaştır. Egzersiz, sistemik ateş veya enjeksiyon bölgesine masaj uygulanması insülinin emilim hızını artırır.
Enjeksiyonda Hangi Yöntemler Kullanılır?
Enjektör, kalem ve pompa biçiminde kullanılır.
Enjektör: Geleneksel uygulama sistemi olan bu yöntem gelişmiş ülkelerde ve ülkemizde giderek daha az kullanılmaktadır. 0.3, 0.5 ve 1 mL’lik enjektörler mevcuttur. Enjektörler 1 I ünite (IU) taksimatlıdır. Çocuklar ve insüline duyarlı bireyler için 0.5 IU’ye ayarlanmış enjektörler de mevcuttur. Genel olarak 8 mm’lik iğneli enjektörler kullanılmaktadır, ayrıca 6 ve 12 mm’lik iğneli enjektörler de bulunmaktadır. Enjektörler için 10 mL’lik (1000 IU insülin içeren) flakonlar kullanılır. Her hasta gereğinde, zorunlu kaldığında enjektör kullanabilmeyi bilmeli ve yanında taşımalıdır.
Kalem (pen): Pratik, güvenli ve doğru insülin uygulama olanağı sağlar, bu nedenlerle daha çok tercih edilmektedir. 300 IU’lik (3 mL hacimli) insülin içeren, kartuşu değişebilen veya tek kullanımlık olarak kullanılabilen insülin kalemleri kullanılmaktadır. Kalemler 1 IU’lik aralıklara göre ayarlanmıştır, çocuklar için 0.5 IU’lik kalemler mevcuttur. İnsülin kalem iğneleri 4 mm, 6 mm, 8 mm veya 12 mm’liktir. Genel kullanımda 8 mm’lik iğneler tercih edilir. 4 mm’lik iğne cilde herhangi bir açı olmaksızın dik uygulanır. Obez hastalarda 12 mm’lik iğnelerin kullanılması gerekebilir.
Pompa: Sürekli cilt altı insülin infüzyon pompaları kullanılmaktadır. 1980’li yılların başında kullanılır hale gelen sistemlerdir. Pompanın rezervuarında depolanan analog insülin, subkütan yerleştirilmiş bir kateter aracılığıyla infüze edilir. Önceden programlanmış oranda bazal insülin olarak sürekli verilir, bolus insülin hastanın yediği karbonhidrat miktarını karşılayacak dozda uygulanır. Bu yaklaşım öğünlere esneklik getirir, hastanın yaşam kalitesini düzeltir. Regüler insülinler kullanıldığında kateter tıkanıklığı, kontrolün hızla kötüleşmesi, diyabetik ketoasidozla sonlanabilir. Bu nedenle akımın kesildiğini gösteren alarmlı sistemler geliştirilmektedir. Günümüzde kullanımına bir başka engel maliyeti ve hasta eğitimi gerektirmesidir.
İnsülin Dozunun Hesaplanması ve Ayarlanması
Başlangıçta vücut ağırlığına göre, kg başına ayarlanır. Ayrıca diyabetli bireyin fenotipi ve fiziksel aktivite durumu ile diyabet komplikasyonları da göz önüne alınmalıdır. Hesaplanan dozun yarısı bazal, yarısı bolus insülin olarak verilir. Uygulamada bir diğer kural, günlük toplam dozun 2/3’ünün gündüz; 1/3’ünün gece süresince verilmesi gereğidir.
• Genel olarak Tip 1 diyabette insülin ihtiyacı 0.5-1.0 U/kg/gün (güvenli başlangıç dozu 0.5-0.8 U/kg/gün); Tip 2 diyabetli bireylerde 0.3-1.5 IU/kg/gün’dür. Tip 2 diyabette dozu belirleyen hastanın fenotipi ve aktivitesidir (Tablo 18). İnsülin dozu belirlenirken hastanın beslenmesi, egzersiz düzeni, eğitim kapasitesi ve yandaş hastalıkları dikkate alınmalı, tedavi bireyselleştirilmelidir.
• Bazal-bolus insülin rejimlerinde günlük gereksinimin yaklaşık yarısı (%40-60) bazal, geri kalan yarısı (%40-60) ise bolus olarak hesaplanarak uygulanır. Bazal-bolus (yoğun) insülin tedavisini uygulayamayacak durumda olan ve konvansiyonel tedavi alması gereken diyabetlilerde günlük dozun 2/3’ünün sabah, 1/3’ünün akşam yemek öncesinde verilmesi önerilir.
• Bazal insülin desteği için 0.1-0.2 IU/kg/gün insülin başlanabilir.
İNSÜLİN TEDAVİ REJİMLERİ
Tedavi rejimi seçerken ideal insülin profilinin sağlanması hedeflenmeli; endojen insülin salınımına benzer bir insülin profili sağlayacak tedaviye erken başlanmalı ve tedavi kişiselleştirilmelidir. Uygulamada daima pratik olanla başlanmalı; seçimde insülinin farmakokinetik özellikleri hastanın yaşam şekli ve yeme alışkanlıkları göz önünde bulundurulmalıdır.
Günlük enjeksiyon sayısına göre insülin tedavi rejimleri yoğun (bazal-bolus, intensif: Günde ≥ 3 doz insülin uygulaması) ve destek insülin (günde tek ya da iki doz insülin uygulaması) olmak üzere ikiye ayrılmaktadır.
1. Bazal-Bolus İnsülin Tedavisi = İntensif = Yoğun İnsülin Tedavisi
Tip 1 diyabetlilerde, diyet ile kontrol altına alınamayan gebelik diyabetinde ve endojen insülin rezervi azalmış Tip 2 diyabetlilerde uygulanmalıdır. Özellikle sık aralıklı = yoğun = intensif insülin tedavisi gören ve A1C düzeyleri normale yakın seyreden Tip 1 diyabet olgularında mikroanjiyopatik komplikasyon riskinin düşük olduğunu gösteren DCCT (Diyabetin Kontrolü ve Komplikasyonları Çalışması) sonuçlarının açıklandığı 1989 yılından beri, daha fizyolojik olan bu yaklaşım şekli daha çok kabul görmekte ve insülin eksikliğinden kaynaklanan tüm sorunların düzeltilmesi amaçlanmaktadır. Aşağıda gösterildiği gibi çoklu doz insülinle ya da subkütan insülin infüzyonu (pompa) şeklinde uygulanabilir.
a. Multipl (çoklu) doz insülin enjeksiyonları (sık aralıklı insülin tedavisi): İnsülin tedavisi düzenlenirken kullanımdaki insülin preparatlarının farmakokinetik özellikleri ve hedeflenen fizyolojik insülinemi göz önünde bulundurulmalıdır. Bu nedenle, gece ve yemek arası dönemler için bazal; yemek sonrası beta-hücresinden salgılanan insülini taklit etmek için bolus insülin uygulaması eğilimi vardır. Bazal-bolus tedavi rejimi adı verilen bu uygulamada hasta eğitimi, evde kendi kendine glukoz ölçümü, kendi tedavisini yönlendirme yaklaşımı başarıya ulaşmanın temel noktalarıdır.
Günde üç kez öğün öncesi hızlı/kısa etkili (bolus) insülin + günde bir kez (tercihan gece) orta/uzun etkili (bazal) insülin veya günde üç kez öğün öncesi hızlı/kısa etkili (bolus) insülin + günde iki kez orta/uzun etkili (bazal) insülin olarak uygulanır. Bazal-bolus insülin tedavisini iki farklı insülin preparatı ile uygulamakta zorluk çeken bazı Tip 2 diyabetli kişilerde günde üç doz analog karışım insülin seçeneği düşünülebilir. Şekil 11’de çoklu doz insülin uygulamasındaki tedavi şeması gösterilmiştir.
b. Sürekli cilt altı insülin infüzyonu (SCİİ): İnsülin pompası ile bazal, bolus ve düzeltme dozlarının yapılmasıdır. Tip 1 diyabetlilerde yoğun insülin tedavisi tercih edilmelidir. En önemli dezavantajı hipoglisemi sıklığının daha fazla oluşu; epizodların sıklığına bağlı olarak gelişen hipoglisemiye duyarsızlık gelişmesidir.
2. İnsülin Destek Tedavisi
Komplikasyonlu veya hipoglisemi riski yüksek yaşlı Tip 1 diyabette, diyetle kontrol altına alınamayan hafif gestasyonel diyabette ve Tip 2 diyabette önerilmektedir. Bifazik insülin tipleri ya da bazal insülin preparatlarıyla uygulanır.
a. Bifazik karışım insülin tedavisi: Günde iki doz orta/uzun etkili + hızlı/kısa etkili karışım insülin olarak ya da hazır karışım insülin preparatları kullanılabilir. Alternatif olarak hasta iki ayrı insülini enjekte edebilir.
b. Bazal insülin desteği: Günde bir veya iki doz orta/uzun etkili (bazal) insülin desteğidir. Tip 2 diyabetlilerde ve bazı gestasyonel diyabet olgularında tercih edilir. Uzun etkili insülin analoglarının gebelikte güvenli kullanımına ilişkin yeterli kanıt yoktur, bu nedenle glargin ve detemir insülinler pregestasyonel diyabet ve gestasyonel diyabet olgularında kullanılmamalıdır. Günümüzde oral antidiyabetik ilaçların orta ya da uzun etkili insülinle desteklenmesi sık yapılan uygulamalardandır.
İnsülin Tedavisinin Komplikasyonları
• Hipoglisemi: İnsülin tedavisinin en önemli ve en sık görülen komplikasyonudur. Sıkı glisemik kontrol ve uzun diyabet süresiyle ilişkilidir. Bazal-bolus insülin tedavisi uygulanan tip 1 diyabetlilerde daha sık görülür. DCCT çalışmasında yoğun insülin tedavisi grubunda hipoglisemi sıklığı konvansiyonel tedavi grubuna göre üç kat daha fazla görülmüştür. İnsülin analogları ile hipoglisemi riski, insan insülinlerine göre biraz daha düşüktür.
• Kilo artışı: İnsülin tedavisinin başlangıcında kaybedilmiş yağ ve kas dokusunun yeniden kazanılması, su ve tuz tutulumu olması ve glukozürinin azalmasına bağlı olarak birkaç kg kadar artış beklenir. Daha sonra hipoglisemi korkusu ve dengesiz beslenme kilo artışının sürmesine neden olabilir.
• Masif hepatomegali: Glikojen depolarının dolmasına bağlıdır, günümüzde nadir görülmektedir.
• Ödem: Ozmotik diürezin azalması ve Na+ tutulumuna bağlı başlangıçta ödem görülebilir.
• Antiinsülin antikorları ve allerji: Günümüzde insan insülinleri ve analog insülin kullanımı ile artık nadir görülen bir komplikasyondur.
• Lipoatrofi/Lipohipertrofi: Saflaştırılması az olan insülinin enjekte edildiği dokuda yağın lokalize kaybıdır. Nadir görülen immünolojik bir olaydır. Lipohipertrofide, sürekli aynı bölgeye enjeksiyon yapılması sonucu görülebilir, enjeksiyon bölgesini değiştirmekle tedavi edilir.
• Kanama, sızma ve ağrı: Enjeksiyonun kapiller damarlanmanın görünmediği bir bölgeye yapılmasıyla kanama önlenir. Enjeksiyon bittikten sonra iğnenin 5-10 saniye kadar cilt altında bekletilmesi veya uzun iğne kullanılmasıyla insülinin sızması azaltılabilir. Özellikle asit insülinler (örn. glargin) ile enjeksiyon sırasında hafif ağrı hissedilebilir, önemsizdir.
• Hiperinsülinemi ile ateroskleroz ve kanser riski: Deneysel çalışmalar hiperinsülinemi-ateroskleroz ilişkisine işaret etse de bu konudaki klinik kanıtlar yeterli değildir.
İnsülin anabolizan bir hormondur. İnsülin reseptörleri yapısal olarak insülin benzeri büyüme hormonlarına (örn. IGF-1) benzer. İnsülinin etki gücü reseptöre afinitesiyle paraleldir. Güçlü insülinlerin insülin ve IGF-1 reseptörlerine afinitesi yüksektir. Bu nedenle uzun yıllar insülin kullanımıyla kanser riski arasında ilişki olabileceği ileri sürülmektedir. Kesitsel çalışmalara dayalı çelişen veriler nedeniyle konu hakkında tartışmalar sürmektedir. Bununla beraber bu konuda yapılmış klinik randomize çalışmalar yoktur.
İnsülin Etkisini Değiştirebilen İlaçlar
Tablo 19’da görülen bazı ilaçlar insülin etkisini artırarak hipoglisemiye, diğer bazı ilaçlar ise insülin etkisini azaltarak (bazıları insülin direnci yaratarak) hiperglisemiye yol açabileceğinden insülin dozlarının ayarlanmasını gerektirir.
V. GÜNÜMÜZDE TİP 1 DİYABETTE TEDAVİ ÖNERİLERİ
Diyabetolog ve endokrinologların günümüzde Tip 1 diyabetli kişilerde uyguladıkları ve önerdikleri tedavi protokolü sık aralıklı (çoklu = bazal-bolus) insülin rejimi ve sürekli cilt altı insülin infüzyonudur. DCCT çalışmasına göre uygun eğitim ve evde kendi kendine glukoz ölçümü ile birlikte insülinin sık aralıklı uygulanması mikrovasküler komplikasyon riskini azaltmaktadır. Çalışma bitiminden sonra gerçekleştirilen EDIC çalışması da intensif tedavi gören gruptaki kardiyovasküler hastalık oranının daha düşük olduğunu vurgulamıştır. Bu nedenle Tip 1 diyabetlilerde uygun eğitim, danışmanlık ve destekle birlikte en uygun tedavi sürekli cilt altı insülin infüzyonudur.
VI. GÜNÜMÜZDE TİP 2 DİYABETTE TEDAVİÖNERİLERİ
Esas aynı kalmakla birlikte son yıllarda Tip 2 diyabet tanısı almış hastaların tedavisine yaklaşım biçimi büyük ölçüde değişmiştir. Yeni önerilere göre glisemik kontrol hedeflerinin daha aşağı çekilmesi ve geleneksel basamaklı tedavinin yerine insülin ve kombinasyon tedavilerine daha erken başlanması benimsenmiştir. Antihiperglisemik tedavi seçiminde glukoz düşürücü etkinin yanında ekstra-glisemik etkiler, güvenlik, tolerabilite ve maliyet de göz önünde bulundurulmalıdır. Türkiye Endokrinoloji ve Metabolizma Derneği (TEMD)’in “Diyabet ve Komplikasyonlarının Tanı, Tedavi ve İzlem Kılavuzu-2011”de Tip 2 diyabet tanısı ile başvuran hastalar için önerilen tedavi algoritması Şekil 12 ve Şekil 13’te gösterilmiştir. Son olarak, yakın dönemde sonuçları açıklanan ACCORD, VADT ve ADVANCE gibi ileriye dönük, geniş katılımlı ve uzun soluklu çalışmalar; Tip 2 diyabete diyabet süresi, daha önceki glisemik kontrol düzeyi, komplikasyon varlığı ve derecesi, eşlik eden hastalıklar, kullanılan diğer ilaçlar ve nihayetinde kişiye özgü yaşam tarzından kaynaklanan özelliklere bakılmaksızın her hastaya aynı hedefleri gözeterek yoğun tedavi uygulanmasının kardiyovasküler olayları ve ölüm riskini artırabileceğini ortaya koymuştur. Bütün bunların ötesinde sıkı metabolik kontrol ile makrovasküler komplikasyon riskinde azalma sağlanamayacağı, ayrıca ilerlemiş ve yerleşmiş mikrovasküler komplikasyonların gerilemeyeceği iyi bilinmektedir.
Bütün bu hususlar, Tip 2 diyabete zemin hazırlayan faktörlerin ve diyabet risk gruplarının iyi bilinmesini ve prediyabetik süreçten itibaren, tanıdan tedaviye her hastanın bireysel olarak ele alınmasının gerekliliğini ortaya koymakta, bir anlamda hekimlik sanatının önemini vurgulamaktadır.
KAYNAKLAR
- International Diabetes Federation. Fifth Diabetes Atlas. IDF Publ., Brussels, 2011.
- Satman I, Yilmaz T, Sengul A, Salman S, Salman F, Uygur S, et al. Population-based study of diabetes and risk characteristics in Turkey: results of the Turkish diabetes epidemiology study (TURDEP). Diabetes Care 2002; 25: 1551-6. [Özet] [Tam Metin] [PDF]
- Satman I, Tutuncu Y, Gedik S, Dinccag N, Karsidag K, Yilmaz T, et al.; The TURDEP-II Study Group. Diabetes epidemic in Turkey: Results of the second population based survey of diabetes and risk characteristics in Turkey (TURDEP-II). Poster: A-11-2498. 47th EASD Annual Meeting, 12-16 Sept 2011, Lisbon, Portugal. Diabetologia 2011; 54(Suppl 1): P2498.
- UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). UK Prospective Diabetes Study (UKPDS) Group. Lancet 1998; 352: 837-53. Erratum in: Lancet 1999; 354: 602. [Özet]
- Holman RR, Paul SK, Bethel MA, Matthews DR, Neil HA. 10-year follow-up of intensive glucose control in type 2 diabetes. N Engl J Med 2008; 359: 1577-89. [Özet] [Tam Metin] [PDF]
- TEMD Diabetes Mellitus ve Komplikasyonlarının Tanı, Tedavi ve İzlem Kılavuzu-2011. (Yazım Komitesi: Satman İ, İmamoğlu Ş, Yılmaz C, Akalın S ve Diabetes Mellitus Çalışma ve Eğitim Grubu). 5. Baskı. Ankara: Bayt Matbaacılık, 2011. [Özet]
- Davis TM, Wright AD, Mehta ZM, Cull CA, Stratton IM, Bottazzo GF, et al. Islet autoantibodies in clinically diagnosed type 2 diabetes: prevalence and relationship with metabolic control (UKPDS 70). Diabetologia 2005; 48: 695-702.
- UK Prospective Diabetes Study Group. UK Prospective Diabetes Study 16: overview of 6 years’ therapy of type II diabetes: a progressive disease. Diabetes 1995; 44: 1249-58. [Özet]
- Terry T, Raravikar K, Chokrungvaranon N, Reaven PD. Does aggressive glycemic control benefit macrovascular and microvascular disease in type 2 diabetes? Insights from ACCORD, ADVANCE, and VADT. Curr Cardiol Rep 2012; 14: 79-88. [Özet]
- Pozzilli P, Guglielmi C, Caprio S, Buzzetti R. Obesity, autoimmunity, and double diabetes in youth. Diabetes Care 2011; 34(Suppl 2): S166-S70. [Özet] [PDF]
- Liorente MD, Urrutia V. Diabetes, psychiatric disorders, and the metabolic effects of antipsychotic medications. Clin Diabet 2006; 24: 18-24.
- Scarsi M, Podvince M, Roth A, Hug H, Kersten S, Albrecht H, et al. Sulphonylureas and glinides exhibit peroxisome proliferator activated receptor gamma activity: a combined virtual screening and biological assay approach. Mol Pharmacol 2007; 2: 398-406. [Özet] [Tam Metin] [PDF]
- Selvin E, Bolen S, Yeh HC, Wiley C, Wilson LM, Marinopoulos SS, et al. Cardiovascular outcomes in trials of diabetes medications: a systematic review. Arch Intern Med 2008; 168: 2070-80. [Özet]
- Sinha Roy R, Bergeron R, Zhu L, et al. Metformin is GLP-1 sectretagog, not a dipeptyl peptidsa-4 inhibitor. Diabetologia 2007; 50(Suppl 1): S284.
- Diabetes Prevention Program Research Group. Reduction in the incidence of type 2 diabetes with life style intervention or metformin. N Engl J Med 2002; 346: 393-403. [Özet] [Tam Metin] [PDF]
- Chiasson JL, Josse RG, Gomis R, Hanefeld M, Karasik A, Laakso M. Acarbose treatment and the risk of cardiovascular disease and hypertension in patients with impaired glucose tolerance. The STOP_NIDDM trial. JAMA 2003; 290: 486-94. [Özet]
- Buse J, Hart K, Minasi L. The PROTECT Study ; final results o a large multicenter postmarketing study in patients with type 2 diabetes. Clin Ther 1998; 20: 257-69. [Özet]
- Ho FL, Liew CF, Cunanan EC, Lee KO. Oral hypoglycaemic agents for diabetes in pregnancy-an appraisal of the current evidence for oral antidiabetic drug use in pregnancy. Ann Acad Med Singapore 2007; 36: 672-8. [Özet] [PDF]
- Gurnell M. Peroxisome prolierator-activarted receptor gama and hyperglycamic agents in type 2 diabetes. In: Khan CR, Weir GC, King GL, Jacobson AM, Moses AC, Smith RJ(eds). Joslin’s Diabetes Mellitus. 14th ed. Philadelphia: Lippicott Williams and Wilkins, 2005: 687-710.
- Niessen SE, Wolski K. Effect of rosiglitazon on the risk of myocardial infarction and death from cardiovascular causes. N Engl J Med 2007; 356: 2457-63. [Özet] [Tam Metin] [PDF]
- Nathan DM, Buse JB, Davidson MB, et al. Medical management of hyperglycaemia in type 2 diabetes. Diabetes Care 2008; 31: 1-11.
- Miller SA, Onge EL. Sitagliptin: a dipeptidyl peptidase IV inhibitor or the treatment of type 2 diabetes. Ann Pharmacotherapy 2006; 40: 1336-43. [Özet]
- Aschner P, Kipnes MS, Lunceford JK, Sanchez M, Mickel C, Williams-Herman DE. Effect of the dipeptidyl peptidase-4 inhibitor sitagliptin as monotherapy on glycemic control in patients with type 2 diabetes. Diabetes Care 2006; 29: 2632-7. [Özet] [Tam Metin] [PDF]
- Nauck MA, Meininger G, Sheng D, Terranella L, Stein PP. Efficacy and safety of the dipeptidyl peptidase-4 inhibitor, sitagliptin, compared with the sulfonylurea, glipizide, in patients with type 2 diabetes inadequately controlled on metformin alone: a randomized, double blind, non-inferiority trial. Diabetes Obes Metab 2007; 9: 194-205. [Özet] [Tam Metin] [PDF]
- Rosenstock J, Baron MA, Dejager S, Mills D, Schweizer A. Comparison of vildagliptin and rosiglitazone monotherapy in patients with type 2 diabetes: a 24-week, double blind, randomized trial. Diabetes Care 2007; 30: 217-23. [Özet] [Tam Metin] [PDF]
- Zinman B, Hoogwerf BJ, Duran Garcia S, Milton DR, Giaconia JM, Kim DD, et al. The effect of adding exenatide to a thiazolidinedione in suboptimally controlled type 2 diabetes: a randomized trial. Ann Intern Med 2007; 146: 477-85. [Özet]
- American Diabetes Association. Executive Summary: Standards of medical care in diabetes-2012. Diabetes Care 2012; 35 (Suppl 1): S4-S10. [Özet] [PDF]
- Inzucchi SE, Porte DJr, Sherwin RS, Baron A (eds). The Diabetes Manual: A Primary Care Companion to Ellenberg and Rifkin’s. 6th ed. New York: McGraw-Hill Medical Publishing Division, 2005.
- Pickup JC, Williams G (eds). Textbook of Diabetes. Volume 1-2. 3rd ed. Blackwell Publishing, Massachusetts, 2003.
- Expert Committee on the Diagnosis and Classification of Diabetes Mellitus. Follow-up report on the diagnosis of diabetes mellitus. Diabetes Care 2003; 26: 3160-7. [Özet] [Tam Metin]
- Canadian Diabetes Association: 2003 Clinical Practice Guidelines for the Prevention and Management of Diabetes in Canada. Canadian J Diabetes 2003; 27 (Suppl 2).
Yazışma Adresi:
Prof. Dr. Nevin DİNÇÇAĞ
İstanbul Üniversitesi İstanbul Tıp Fakültesi,
İç Hastalıkları Anabilim Dalı,
Endokrinoloji ve Metabolizma Hastalıkları Bilim Dalı,
34093 Fatih/Çapa, İSTANBUL
E-posta: drdinccag@superonline.com